引言:近日��,藥監(jiān)總局發(fā)布2019年度醫(yī)療器械注冊工作報告���,報告中包括了哪些重要信息?一起來了解�。

2019年度醫(yī)療器械注冊工作報告
2019年,國家藥監(jiān)局以習近平新時代中國特色社會主義思想為指導�����,全面貫徹“四個最嚴”要求�,以保護和促進公眾用械安全為使命����,持續(xù)深化醫(yī)療器械審評審批制度改革,推動監(jiān)管科學研究����,堅持風險管理,強化責任落實�,推進智慧監(jiān)管,著力提升醫(yī)療器械注冊審評審批的質量與效率��。
一�、醫(yī)療器械注冊工作情況
?�。ㄒ唬┽t(yī)療器械法規(guī)體系進一步完善
1.積極推進醫(yī)療器械監(jiān)督管理條例修訂��。配合司法部開展重點問題實地調研并對條例進一步修改完善��,同步啟動配套規(guī)章���、規(guī)范性文件的制修訂。
2.發(fā)布《定制式醫(yī)療器械監(jiān)督管理規(guī)定(試行)》(2019年第53號公告)�����。明確定制式醫(yī)療器械的定義���、備案�、設計��、加工��、使用���、監(jiān)督管理等方面要求���,進一步鼓勵定制式醫(yī)療器械的創(chuàng)新研發(fā)��,滿足臨床罕見個性化需求���。
3.持續(xù)推進醫(yī)療器械技術審查指導原則制修訂。發(fā)布《醫(yī)療器械附條件批準上市指導原則》等57項醫(yī)療器械技術審查指導原則�,統(tǒng)一審查尺度,提升各級藥品監(jiān)管部門審查水平��。
?��。ǘ┽t(yī)療器械審評審批制度改革持續(xù)深入
1.優(yōu)化臨床試驗審批���。發(fā)布《關于調整醫(yī)療器械臨床試驗審批程序的公告》(2019年第26號公告),進一步優(yōu)化臨床試驗審批程序�,由“明示”許可調整為“默示”許可�����。
2.繼續(xù)擴大免于進行臨床試驗醫(yī)療器械目錄����。發(fā)布《關于公布新增和修訂的免于進行臨床試驗醫(yī)療器械目錄的通告》(2019年第91號公告),新增148項醫(yī)療器械產品和23項體外診斷試劑產品免于進行臨床試驗�,對48項醫(yī)療器械產品和4項體外診斷試劑產品名稱和描述進行了修訂���。目前免于進行臨床試驗醫(yī)療器械目錄包含1003項,體外診斷試劑目錄包含416項�����,合計達到1419項�。
3.持續(xù)做好創(chuàng)新醫(yī)療器械審批工作。2019年共有36個創(chuàng)新產品和12個優(yōu)先審批產品進入“綠色通道”�����。批準正電子發(fā)射斷層掃描及磁共振成像系統(tǒng)等19個創(chuàng)新醫(yī)療器械��,中空纖維膜血液透析濾過器等10項優(yōu)先產品上市����,促進醫(yī)療器械產業(yè)創(chuàng)新發(fā)展,滿足人民群眾使用高水平醫(yī)療器械需要�����。
4.擴大醫(yī)療器械注冊人制度試點�。印發(fā)《國家藥監(jiān)局關于擴大醫(yī)療器械注冊人制度試點工作的通知》,將醫(yī)療器械注冊人制度試點推至北京����、江蘇�、浙江等21個省�����、自治區(qū)和直轄市���。2019年共有22家企業(yè)的93個產品按照注冊人制度試點獲批����,其中包括跨省委托生產和第三類醫(yī)療器械通過注冊人制度委托生產等不同情況�。進一步釋放醫(yī)療器械注冊人制度紅利,鼓勵醫(yī)療器械創(chuàng)新���,落實主體責任�,為全面實施醫(yī)療器械注冊人制度提供重要支撐�。
?�。ㄈ┽t(yī)療器械基礎工作不斷夯實
1.醫(yī)療器械標準體系進一步健全��。2019年���,國家藥監(jiān)局下達108項標準制修訂項目����,其中國家標準15項、行業(yè)標準93項���。發(fā)布行業(yè)標準72項�����。截止2019年底����,醫(yī)療器械現(xiàn)行有效標準共1671項���,其中國家標準220項�����,行業(yè)標準1451項����,我國標準與國際標準一致性程度達到90.4%。
2.分類和命名工作持續(xù)完善���。優(yōu)化藥械組合產品屬性界定工作��,發(fā)布《關于調整藥械組合產品屬性界定有關事項的通告》�����。制定分類目錄動態(tài)調整工作程序����。分3批公布1073項分類界定結果��,指導各方精準分類���。發(fā)布《醫(yī)療器械通用名稱命名指導原則》��,進一步規(guī)范醫(yī)療器械通用名稱�����。
?。ㄋ模┽t(yī)療器械智慧監(jiān)管初見成效
1.推進注冊電子申報����。印發(fā)《關于實施醫(yī)療器械注冊電子申報的公告》,建立注冊電子申報信息系統(tǒng)(eRPS)���,實現(xiàn)注冊申報網上辦理��。2019年����,共有7512項注冊申請通過線上提交����。
2.開展立卷審查。實現(xiàn)審評項目智能分配�,簡單項目和復雜項目分級審評,首次注冊���、復雜變更和臨床試驗審批立卷審查����,以臨床為導向的分段審評制度和復雜項目管理人制度逐步建立���。
3.實施醫(yī)療器械唯一標識����。印發(fā)《醫(yī)療器械唯一標識系統(tǒng)規(guī)則》和相關標準,完成醫(yī)療器械唯一標識數據庫一期工程建設����,賦予產品“電子身份證”。強化源頭賦碼�����,探索從源頭生產到臨床使用全鏈條聯(lián)動����。會同國家衛(wèi)生健康委印發(fā)《醫(yī)療器械唯一標識系統(tǒng)試點工作方案》,聯(lián)合開展試點��。發(fā)布第一批醫(yī)療器械唯一標識工作有關事項的通告�����,明確品種范圍�����、進度安排和工作要求����,分步推動醫(yī)療器械唯一標識工作有序開展���。
?�。ㄎ澹┡R床試驗和注冊資料管理繼續(xù)加強
1.繼續(xù)開展醫(yī)療器械臨床試驗監(jiān)督檢查����。分2批對20個醫(yī)療器械臨床試驗項目進行監(jiān)督檢查,對16個注冊項目開展臨床試驗樣本真實性延伸核查��。
2.積極推動醫(yī)療器械臨床試驗機構備案�。截止2019年底,全國已有839家臨床試驗機構備案����。對管理者、項目負責人和臨床試驗技術人員開展三期培訓��。
3.嚴厲打擊提供虛假注冊資料注冊行為��。根據相關線索組織對深圳萊福百泰醫(yī)療科技有限公司開展核查���,對深圳萊福百泰醫(yī)療科技有限公司所提交的電子上消化道內窺鏡和電子下消化道內窺鏡兩個產品不予注冊�。
(六)監(jiān)管科學研究穩(wěn)步推進
1.積極推進監(jiān)管科學研究��。啟動中國藥品監(jiān)管科學行動計劃��。首批啟動項目包括藥械組合產品技術評價研究��、人工智能醫(yī)療器械安全有效性評價研究����、醫(yī)療器械新材料監(jiān)管科學研究、真實世界數據用于醫(yī)療器械臨床評價的方法學研究等項目��。在四川大學���、華南理工大學設立國家局監(jiān)管科學研究基地����,推動醫(yī)療器械監(jiān)管科學研究工作�。
2.推動醫(yī)療器械臨床真實世界數據應用試點。結合監(jiān)管科學行動計劃項目�����,推動臨床真實世界數據應用試點��,依托重點地區(qū),制定試點方案��,確定試點產品��,制定《真實世界數據用于醫(yī)療器械臨床評價技術指導原則》�����。
?�。ㄆ撸﹪H交流合作取得實效
1.國際交流成果豐碩�。參加國際醫(yī)療器械監(jiān)管機構論壇(IMDRF)第16次管理委員會會議���,經IMDRF成員國一致同意�����,會議批準我國牽頭的臨床評價工作組“臨床證據–關鍵定義和概念”“臨床評價”“臨床研究”三份指南文件�����,這是自中國加入IMDRF后第一次由中國藥品監(jiān)管機構牽頭組織編寫的指南文件����。管理委員會同時贊成中國牽頭的工作組提出的“上市后臨床隨訪研究”擴展項目立項。管理委員會一致同意中國加入國家監(jiān)管機構報告信息交流機制�����,與成員國共同分享醫(yī)療器械產品相關安全信息�����,共同應對全球醫(yī)療器械風險挑戰(zhàn)�����。此外��,中國作為標準工作組聯(lián)席主席國�,在本次會議上派代表向管理委員會和業(yè)界介紹了標準工作組工作進展,研究成果《標準認可和使用情況分析報告》和《認可標準清單》經管理委員會全體成員一致同意通過��。
2.參加第24屆亞洲醫(yī)療器械法規(guī)協(xié)調會(AHWP)年會�。作為AHWP副主席和兩個工作組主席,介紹中國醫(yī)療器械注冊和監(jiān)管體系最新進展�����,主持工作組工作討論和法規(guī)協(xié)調工作�����,充分發(fā)揮我國在區(qū)域醫(yī)療器械監(jiān)管中的作用,積極推進亞洲法規(guī)協(xié)調工作��。
二����、醫(yī)療器械注冊申請受理情況
2019年,國家藥監(jiān)局依職責共受理醫(yī)療器械首次注冊���、延續(xù)注冊和許可事項變更注冊申請9104項,與2018年相比注冊受理項目增加37.8%�����。
?�。ㄒ唬┱w情況
受理境內第三類醫(yī)療器械注冊申請3511項����,受理進口醫(yī)療器械注冊申請5593項。
按注冊品種區(qū)分�����,醫(yī)療器械注冊申請5877項,體外診斷試劑注冊申請3227項���。
按注冊形式區(qū)分��,首次注冊申請1693項��,占全部醫(yī)療器械注冊申請的18.6%���;延續(xù)注冊申請5081項,占全部醫(yī)療器械注冊申請的55.8%����;許可事項變更注冊申請2330項,占全部醫(yī)療器械注冊申請的25.6%��。注冊形式比例情況見圖1���。

(二)分項情況
1.境內第三類醫(yī)療器械注冊受理情況
境內第三類醫(yī)療器械注冊受理共3511項�����,與2018年相比大幅增加47.4%���。其中����,醫(yī)療器械注冊申請2154項��,體外診斷試劑注冊申請1357項��。
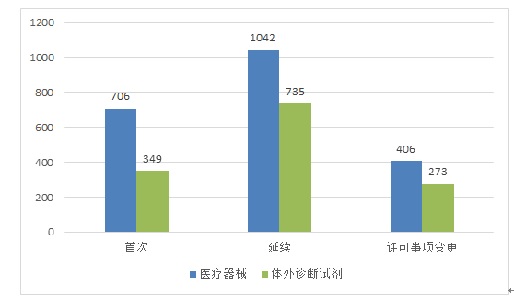
從注冊形式看��,首次注冊1055項��,占全部境內第三類醫(yī)療器械注冊申請數量的30.0%�;延續(xù)注冊1777項,占全部境內第三類醫(yī)療器械注冊申請數量的50.6%�����;許可事項變更679項�,占全部境內第三類醫(yī)療器械注冊申請數量的19.3%��。注冊形式分布情況見圖2��。
2.進口第二類醫(yī)療器械注冊受理情況
進口第二類醫(yī)療器械注冊受理共3053項�����,與2018年相比增加43.7%。其中醫(yī)療器械注冊申請1559項�,體外診斷試劑注冊申請1494項。
從注冊形式看�,首次注冊358項,占全部進口第二類醫(yī)療器械注冊申請數量的11.7%�;延續(xù)注冊1847項,占全部進口第二類醫(yī)療器械注冊申請數量的60.5%�����;許可事項變更848項��,占全部進口第二類醫(yī)療器械注冊申請數量的27.8%�。注冊形式分布情況見圖3。

3.進口第三類醫(yī)療器械注冊受理情況
進口第三類醫(yī)療器械注冊受理共2540項���,與2018年相比增加20.9%�。其中醫(yī)療器械注冊申請2164項�����,體外診斷試劑注冊申請376項�����。
從注冊形式看,首次注冊280項���,占全部進口第三類醫(yī)療器械注冊申請數量的11.0%�����;延續(xù)注冊1457項����,占全部進口第三類醫(yī)療器械注冊申請數量的57.4%�;許可事項變更803項,占全部進口第三類醫(yī)療器械注冊申請數量的31.6%�。注冊形式分布情況見圖4。

三�、醫(yī)療器械注冊審批情況
2019年,國家藥監(jiān)局共批準醫(yī)療器械首次注冊��、延續(xù)注冊和變更注冊8471項��,與2018年相比注冊批準總數量增長53.2%�。其中���,首次注冊1726項��,延續(xù)注冊4504項�,許可事項變更2241項。
2019年��,企業(yè)自行撤回注冊申請210項����,自行注銷注冊證書66項。
近6年國家藥監(jiān)局批準醫(yī)療器械注冊情況見圖5���。

(一)整體情況
2019年��,國家藥監(jiān)局批準境內第三類醫(yī)療器械注冊3179項���,與2018年相比增加86.0%,進口醫(yī)療器械5292項��,與2018年相比增加38.6%��。
按照注冊品種區(qū)分����,醫(yī)療器械5226項�,占全部醫(yī)療器械注冊數量的61.7%�;體外診斷試劑3245項,占全部醫(yī)療器械注冊數量的38.3%���。
按照注冊形式區(qū)分�����,首次注冊1726項���,占全部醫(yī)療器械注冊數量的20.4%;延續(xù)注冊4504項��,占全部醫(yī)療器械注冊數量的53.2%����;許可事項變更注冊2241項,占全部醫(yī)療器械注冊數量的26.4%���。注冊形式比例情況見圖6�?��!����。ǘ┓猪椙闆r
1.境內第三類醫(yī)療器械注冊審批情況
境內第三類醫(yī)療器械注冊3179項����。其中,醫(yī)療器械2014項���,體外診斷試劑1165項��。
從注冊形式看���,首次注冊1067項,占全部境內第三類醫(yī)療器械注冊數量的33.6%�����,延續(xù)注冊1465項����,占全部境內第三類醫(yī)療器械注冊數量的46.1%;許可事項變更注冊647項�,占全部境內第三類醫(yī)療器械注冊數量的20.4%。
2.進口第二類醫(yī)療器械注冊審批情況
進口第二類醫(yī)療器械注冊2754項����。其中�����,醫(yī)療器械注冊1521項���,體外診斷試劑注冊1233項。
從注冊形式看��,首次注冊375項���,占全部進口第二類醫(yī)療器械注冊數量的13.6%�����;延續(xù)注冊1622項�,占全部進口第二類醫(yī)療器械注冊數量的58.9%����;許可事項變更注冊757項,占全部進口第二類醫(yī)療器械注冊數量的27.5%�。注冊形式分布情況見圖8。
3.進口第三類醫(yī)療器械注冊審批情況
進口第三類醫(yī)療器械注冊2538項。其中���,醫(yī)療器械注冊2206項����,體外診斷試劑注冊332項�����。
從注冊形式看��,首次注冊284項��,占全部進口第三類醫(yī)療器械注冊數量的11.2%��;延續(xù)注冊1417項��,占全部進口第三類醫(yī)療器械注冊數量的55.8%���;許可事項變更注冊837項,占全部進口第三類醫(yī)療器械注冊數量的33.0%���。注冊形式分布情況見圖9�。
(三)首次注冊項目月度審批情況
2019年����,國家藥監(jiān)局共批準醫(yī)療器械首次注冊1726項����,月度審批情況見圖10�。
(四)具體批準品種種類分析
注冊的境內第三類醫(yī)療器械,除體外診斷試劑外��,共涉及《醫(yī)療器械分類目錄》中19個子目錄的產品�。
注冊數量前五位的境內第三類醫(yī)療器械是:無源植入器械、注輸�、護理和防護器械、神經和心血管手術器械�����、醫(yī)用成像器械和有源手術器械�����。
注冊的進口醫(yī)療器械��,除體外診斷試劑外��,共涉及《醫(yī)療器械分類目錄》中23個子目錄的產品。
注冊數量前五位的進口醫(yī)療器械�,主要是:醫(yī)用成像器械、口腔科器械����、無源植入器械、臨床檢驗器械����、神經和心血管手術器械���。
(五)進口醫(yī)療器械國別情況
2019年�����,美國��、德國����、日本�、韓國、瑞士醫(yī)療器械在中國醫(yī)療器械進口產品首次注冊數量排前5位���,注冊產品數量約占2019年進口產品首次注冊總數量的75.4%�,與2018年相比基本持平。
(六)境內第三類醫(yī)療器械省份分析
從2019年境內第三類醫(yī)療器械注冊情況看����,相關注冊產品生產企業(yè)主要集中在沿海經濟較發(fā)達省份。其中��,江蘇����、北京、廣東����、上海、浙江是境內第三類醫(yī)療器械首次注冊數量排前五名的省份�����,占2019年境內第三類醫(yī)療器械首次注冊數量的69.1%�,與2018年相比略有增加。