經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品可采用TPU��、聚氯乙烯�����、硅橡膠等材料制成����,目前已上市產(chǎn)品常用材料為TPU。通常由頭端�、管體、接頭����、接頭蓋、導(dǎo)絲等組成��。根據(jù)產(chǎn)品結(jié)構(gòu)可分為單腔����、雙腔、三腔等�����,頭端可有直插型、螺旋型���、重力型��、球囊等不同設(shè)計�����;接口有扣蓋��,有利于保持清潔��;外壁帶有數(shù)字刻度���,可有效指示產(chǎn)品在體內(nèi)的使用長度;管壁使用射線可探測材料�,具有顯影定位功能。
經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品可采用TPU����、聚氯乙烯、硅橡膠等材料制成����,目前已上市產(chǎn)品常用材料為TPU�。通常由頭端��、管體�、接頭�、接頭蓋、導(dǎo)絲等組成��。根據(jù)產(chǎn)品結(jié)構(gòu)可分為單腔��、雙腔�����、三腔等����,頭端可有直插型、螺旋型����、重力型、球囊等不同設(shè)計���;接口有扣蓋�����,有利于保持清潔�����;外壁帶有數(shù)字刻度�,可有效指示產(chǎn)品在體內(nèi)的使用長度;管壁使用射線可探測材料����,具有顯影定位功能。
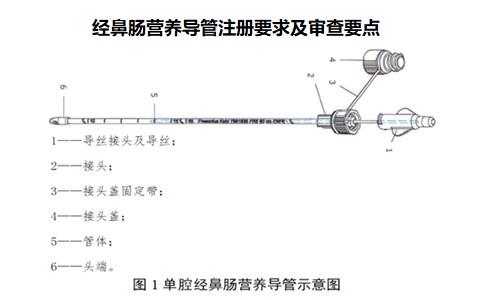
經(jīng)鼻腸營養(yǎng)導(dǎo)管通常由鼻腔經(jīng)食道插入胃����,在胃腸蠕動的推動下滑移進入十二指腸或空腸內(nèi),或借助胃鏡/十二指腸鏡輔助插入十二指腸或空腸�,并經(jīng)X射線顯影等方式確定置管位置,與相關(guān)給營養(yǎng)器械配合����,用于向胃腸道引入營養(yǎng)液等,部分多腔鼻腸管還可用于胃部沖洗等����。
1.經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品的適用范圍���、禁忌證
1.1適用范圍
醫(yī)療器械注冊申請人應(yīng)當明確產(chǎn)品的適用范圍,其描述應(yīng)與申報產(chǎn)品的性能��、功能相符�����,并應(yīng)與臨床評價資料結(jié)論一致���。如:用于經(jīng)鼻向胃腸道引入營養(yǎng)液等。部分可實現(xiàn)沖洗等其他輔助功能���。
1.2預(yù)期使用環(huán)境
明確該產(chǎn)品預(yù)期使用的地點�����,如醫(yī)療機構(gòu)等�?���?赡苡绊懫浒踩院陀行缘沫h(huán)境條件,如溫度���、濕度���、壓力��、海拔等���。1.3適用人群
適用人群建議說明目標患者人群信息,患者選擇標準���,重要考慮因素等�����。
1.4禁忌證:產(chǎn)品材料有過敏史者��,食道下段靜脈曲張患者�����、食道出血患者��、食道梗阻患者�����、腸道吸收障礙患者等其他不宜采用經(jīng)鼻腸營養(yǎng)管飼的患者�����。
2.經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品技術(shù)要求及檢驗報告
2.1經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品技術(shù)要求
應(yīng)當按照《醫(yī)療器械產(chǎn)品技術(shù)要求編寫指導(dǎo)原則》的規(guī)定編制產(chǎn)品技術(shù)要求��,技術(shù)指標引用標準應(yīng)當為現(xiàn)行有效版本�。
經(jīng)鼻腸營養(yǎng)導(dǎo)管基本技術(shù)性能指標包括但不限于以下內(nèi)容����,申請人可根據(jù)產(chǎn)品自身特點,參考相應(yīng)的國家���、行業(yè)標準制定產(chǎn)品技術(shù)要求����,如有不適用條款(包括國家標準��、行業(yè)標準要求)���,申請人應(yīng)在申報資料中說明理由�����。
2.1.1外觀 :經(jīng)鼻腸營養(yǎng)導(dǎo)管應(yīng)清潔��、無異物��,不應(yīng)有表面缺陷和加工缺陷�����;導(dǎo)絲頭端應(yīng)圓鈍�����。
2.1.2尺寸:外徑��、內(nèi)徑���、長度及允差等�。
應(yīng)給出產(chǎn)品的示意圖�。
2.1.3連接件(拉伸性能、液體泄漏)
應(yīng)符合YY 0483要求��。
2.1.4拉伸性能:應(yīng)符合YY 0483要求�。
2.1.5管身刻度的要求。
2.1.6抗彎曲性能。
2.1.7配合性能��。
2.1.8耐腐蝕性(若適用)����。
2.1.9化學(xué)性能。
根據(jù)不同材料特性��,由企業(yè)決定具體的化學(xué)性能要求(如:酸堿度�、紫外吸光度、還原物質(zhì)���、蒸發(fā)殘渣��、重金屬、過氧化物等����,具體指標的選擇可以參照相應(yīng)的國家、行業(yè)標準及已上市同類產(chǎn)品情況)���。用環(huán)氧乙烷滅菌的產(chǎn)品應(yīng)規(guī)定環(huán)氧乙烷殘留量的要求���。
2.1.10射線可探測性(也可使用其他定位方式,如:電磁導(dǎo)航等)。
2.1.11產(chǎn)品應(yīng)無菌����。
2.1.12根據(jù)產(chǎn)品宣稱的技術(shù)特點制定的其他性能要求。
耐壓性(若適用)����;
涂層(若適用):摩擦力等;
帶球囊的產(chǎn)品應(yīng)符合YY/T 0817要求�。
2.2經(jīng)鼻腸營養(yǎng)導(dǎo)管注冊產(chǎn)品檢驗報告
提供檢驗樣品型號/規(guī)格的選擇依據(jù)。所檢驗型號/規(guī)格需為能夠代表本注冊單元內(nèi)其他型號/規(guī)格的典型產(chǎn)品��。當申報產(chǎn)品包括多個型號規(guī)格���,需綜合考慮經(jīng)鼻腸營養(yǎng)導(dǎo)管的原材料���、結(jié)構(gòu)組成、包裝方式��、滅菌方式��、生產(chǎn)工藝和預(yù)期用途等影響因素����。一個型號不能完全覆蓋時,應(yīng)選擇其他型號進行相關(guān)性能的補充性檢測。注意典型型號/規(guī)格不一定是臨床常用型號/規(guī)格�����。