輸尿管支架在我國屬于第二類醫(yī)療器械注冊?產(chǎn)品��,通常由硅橡膠�����、聚氨酯或其他聚合物制造��。產(chǎn)品放置于腎盂與膀胱之間�����,用于對人體輸尿管進(jìn)行支撐和引流��。一起來了解輸尿管支架注冊要求���。
輸尿管支架在我國屬于第二類醫(yī)療器械注冊產(chǎn)品�����,通常由硅橡膠�、聚氨酯或其他聚合物制造。產(chǎn)品放置于腎盂與膀胱之間����,用于對人體輸尿管進(jìn)行支撐和引流。一起來了解輸尿管支架注冊要求�����。
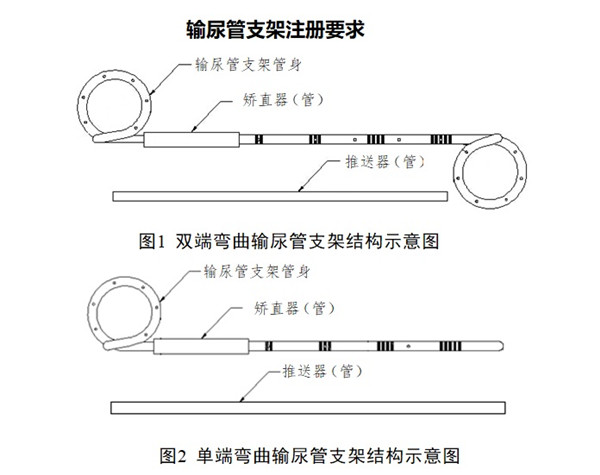
輸尿管支架注冊要求及審評要點(diǎn):
1.輸尿管支架注冊產(chǎn)品的結(jié)構(gòu)及組成
輸尿管支架通常由硅橡膠����、聚氨酯或其他聚合物制造,單端或雙端有環(huán)狀彎曲�����,可包含推送器(管)�、矯直器(管)�����、導(dǎo)絲等配件,也可含有縫線�����、涂層�����、顯影材料等結(jié)構(gòu)����。輸尿管支架可按形狀(單端彎曲或雙端彎曲)、長度����、管徑等不同分為若干型號與規(guī)格,以無菌形式提供�。放置于腎盂與膀胱之間,用于對人體輸尿管進(jìn)行支撐和引流�����。體內(nèi)滯留時間小于30天。
2.輸尿管支架注冊產(chǎn)品技術(shù)要求的主要性能指標(biāo)
產(chǎn)品技術(shù)要求的制訂應(yīng)符合《醫(yī)療器械產(chǎn)品技術(shù)要求編寫指導(dǎo)原則》的要求��。企業(yè)應(yīng)根據(jù)自身產(chǎn)品的技術(shù)特征和臨床使用情況來確定產(chǎn)品安全有效的性能指標(biāo)和檢驗(yàn)方法��。對宣稱的產(chǎn)品的所有技術(shù)參數(shù)和功能���,應(yīng)在產(chǎn)品技術(shù)要求中予以規(guī)定���。輸尿管支架產(chǎn)品的部分檢驗(yàn)方法,可參考相應(yīng)行業(yè)標(biāo)準(zhǔn)YY/T 0872《輸尿管支架試驗(yàn)方法》��。若對標(biāo)準(zhǔn)中的試驗(yàn)方法有所修改���,應(yīng)說明修改的內(nèi)容及原因��,并提交驗(yàn)證資料��。通常應(yīng)考慮(但不限于)以下性能指標(biāo)���。
2.1物理性能:
2.1.1外觀
2.1.2尺寸
2.1.3固定強(qiáng)度
2.1.4斷裂強(qiáng)度
2.1.5伸長率
2.1.6動態(tài)摩擦力(適用于聲稱“低摩擦”的產(chǎn)品)
2.1.7與配件的配合性能
2.1.8耐彎曲
2.1.9縫線結(jié)合強(qiáng)度(適用于帶縫線可取出的產(chǎn)品)
2.2化學(xué)性能:
2.2.1 pH
2.2.2重金屬
2.2.3紫外吸光度
2.2.4還原物質(zhì)
2.2.5蒸發(fā)殘?jiān)?/span>
2.2.6用環(huán)氧乙烷滅菌的產(chǎn)品應(yīng)規(guī)定環(huán)氧乙烷殘留量的要求。
2.2.7由硅橡膠制成的產(chǎn)品可參考YY 0334《硅橡膠外科植入物通用要求》制訂產(chǎn)品的化學(xué)性能要求�����。
2.3無菌。
2.4細(xì)菌內(nèi)毒素(如適用)�。
2.5如產(chǎn)品包含相關(guān)配件���,還應(yīng)制訂配件的性能指標(biāo)�����。如金屬導(dǎo)絲的耐腐蝕等�����。
3.輸尿管支架注冊單元劃分的原則
根據(jù)《醫(yī)療器械分類目錄》及有關(guān)的分類界定文件��,產(chǎn)品管理類別為Ⅱ類�����,分類編碼為14-05-05�����。
醫(yī)療器械產(chǎn)品的注冊單元原則上以技術(shù)結(jié)構(gòu)���、性能指標(biāo)和預(yù)期用途為劃分依據(jù)�����。不同原材料��、不同技術(shù)結(jié)構(gòu)產(chǎn)品應(yīng)劃分為不同醫(yī)療器械注冊單元���。
例如:硅橡膠材料和聚氨酯材料制成的輸尿管支架應(yīng)劃分為不同注冊單元。