為規(guī)范醫(yī)療器械注冊(cè)管理���,根據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院令第739號(hào))和《醫(yī)療器械注冊(cè)與備案管理辦法》(國(guó)家市場(chǎng)監(jiān)督管理總局令第47號(hào))�,國(guó)家藥監(jiān)局組織制定了醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式(見(jiàn)附件)�,現(xiàn)予公布,自2022年1月1日起施行�。原國(guó)家食品藥品監(jiān)督管理總局發(fā)布的《關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》(原國(guó)家食品藥品監(jiān)督管理總局公告2014年第43號(hào))同時(shí)廢止。 特此公告����。 附件:1.中華人民共和國(guó)醫(yī)療器械注冊(cè)證格式 2.中華人民共和國(guó)醫(yī)療器械變更注冊(cè)(備案)文件(格式) 3.國(guó)家藥品監(jiān)督管理局醫(yī)療器械臨床試驗(yàn)審批意見(jiàn)單(格式).doc 4.醫(yī)療器械注冊(cè)申報(bào)資料和批準(zhǔn)證明文件格式要求.doc 5.醫(yī)療器械注冊(cè)申報(bào)資料要求及說(shuō)明.doc 6.醫(yī)療器械延續(xù)注冊(cè)申報(bào)資料要求及說(shuō)明.doc 7.醫(yī)療器械變更備案/變更注冊(cè)申報(bào)資料要求及說(shuō)明.doc 8.醫(yī)療器械臨床試驗(yàn)審批申報(bào)資料要求及說(shuō)明.doc 9.醫(yī)療器械安全和性能基本原則清單.doc 例如:中華人民共和國(guó)醫(yī)療器械注冊(cè)證格式 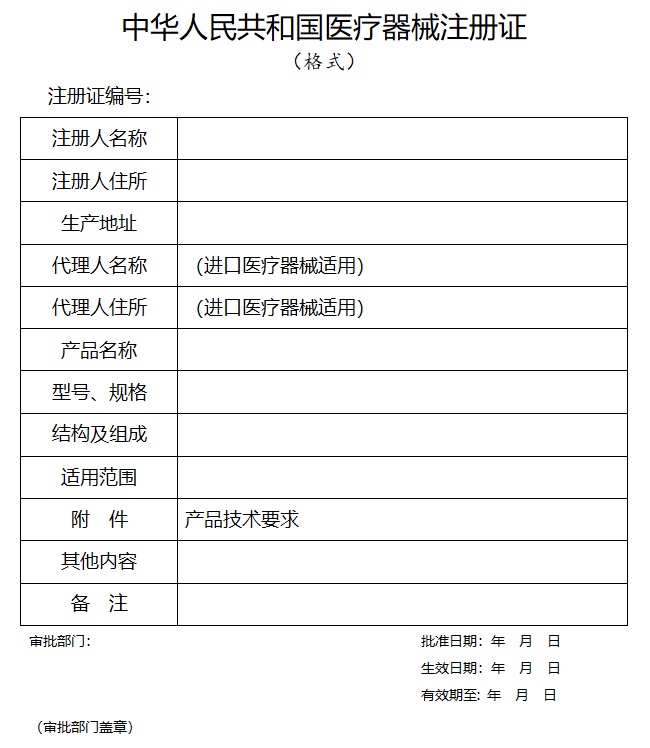
國(guó)家藥監(jiān)局 2021年9月29日
|