盡管商業(yè)環(huán)境復雜多變,盡管很多次真理被假象覆蓋�;盡管很多次被誤解、被非議��。但是我們一直堅信��、堅持���、堅守對的邏輯���;一直做市場誠信機制守護者;一直秉持基本的個人道德���、執(zhí)業(yè)操守�����,及公司信條工作�����。感謝藥監(jiān)總局發(fā)聲�,為市場帶來官方、權(quán)威的注釋����。
引言:盡管商業(yè)環(huán)境復雜多變,盡管很多次真理被假象覆蓋���;盡管很多次被誤解�、被非議�。但是我們一直堅信、堅持��、堅守對的邏輯���;一直做市場誠信機制守護者�����;一直秉持基本的個人道德�、執(zhí)業(yè)操守�,及公司信條工作。感謝藥監(jiān)總局發(fā)聲,為市場帶來官方�����、權(quán)威的注釋��。

口罩等防疫用品出口歐盟及美國市場認證信息指南
為做好新冠肺炎疫情防控和經(jīng)濟社會發(fā)展工作����,支持企業(yè)復工復產(chǎn)��,針對企業(yè)不熟悉防疫物資出口政策等實際問題���,現(xiàn)就口罩等防疫用品出口歐盟及美國的相關(guān)準入要求及梳理的國內(nèi)具有相應資質(zhì)能力的認證機構(gòu)名錄提供如下信息指南�����,供企業(yè)參考��。
一�、歐盟對口罩等防疫用品準入要求
?。ㄒ唬┛谡?/span>
歐盟根據(jù)用途將口罩分為兩類:醫(yī)用口罩和個人防護口罩。
1.醫(yī)用口罩
醫(yī)用口罩需按照歐盟醫(yī)療器械指令93/42/EEC(MDD)或歐盟醫(yī)療器械條例EU2017/745(MDR)加貼CE標志����,對應的標準是EN14683��。根據(jù)口罩產(chǎn)品無菌或非無菌狀態(tài)�����,采取的合格評定模式也不同��。
?��。?)無菌醫(yī)用口罩:必須由授權(quán)公告機構(gòu)進行CE認證。
?�。?)非無菌醫(yī)用口罩:企業(yè)只需進行CE自我符合性聲明�,不需要通過公告機構(gòu)認證。在準備好相應文件及測試報告等資料后�,即可自行完成符合性聲明。
2. 個人防護口罩
個人防護口罩不屬于醫(yī)療器械���,但需符合歐盟個人防護設(shè)備條例EU2016/425(PPE)要求��,由授權(quán)公告機構(gòu)進行CE認證并頒發(fā)證書�,對應的標準是EN149����。
?�。ǘ┓雷o服
防護服也分為醫(yī)用防護服和個人防護服����,管理要求與口罩基本類似����。醫(yī)用防護服按照醫(yī)療器械管理,其中無菌醫(yī)用防護服需按照歐盟醫(yī)療器械指令93/42/EEC(MDD)或歐盟醫(yī)療器械條例EU2017/745(MDR)獲得CE認證���,非無菌醫(yī)用防護服只需進行CE自我聲明。個人防護服需按照歐盟個人防護設(shè)備條例EU2016/425(PPE)獲得CE認證���。
?���。ㄈ?歐盟公告機構(gòu)查詢地址
1.歐盟醫(yī)療器械指令93/42/EEC(MDD)授權(quán)的公告機構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
2.歐盟醫(yī)療器械條例EU 2017/745(MDR)授權(quán)的公告機構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
3.歐盟個人防護裝備條例EU2016/425(PPE)授權(quán)的公告機構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=155501
二��、美國對口罩等防疫用品準入要求
?���。ㄒ唬┛谡?/span>
美國對醫(yī)用口罩和防護口罩同樣區(qū)分管理,其中醫(yī)用口罩由美國食品藥品監(jiān)督管理局(FDA)管理,而個人防護口罩則由美國國家職業(yè)安全衛(wèi)生研究所(NIOSH)管理�。
1. 醫(yī)用口罩
醫(yī)用口罩需通過FDA注冊,企業(yè)直接向FDA官網(wǎng)申請并提交相關(guān)材料����。此外還有兩種可選途徑:
(1)已經(jīng)獲得NIOSH注冊的N95口罩�����,在產(chǎn)品生物學測試��、阻燃測試和血液穿透測試通過的情況下���,可以豁免產(chǎn)品上市登記(510K)��,直接進行FDA工廠注冊和醫(yī)療器械列名�。
?���。?)如果獲得持有510K的制造商的授權(quán),可以作為其代工廠使用其510K批準號進行企業(yè)注冊和器械列名�。
2. 個人防護口罩
防護口罩需通過NIOSH注冊,企業(yè)直接在NIOSH官網(wǎng)申請����。
?����。ǘ┓雷o服
對醫(yī)用防護服和個人防護服的管理也類似于口罩的管理方式����,其中醫(yī)用防護服由美國食品藥品監(jiān)督管理局(FDA)管理���,而個人防護服由美國國家職業(yè)安全衛(wèi)生研究所(NIOSH)管理�。企業(yè)直接在FDA或NIOSH進行注冊申請����。
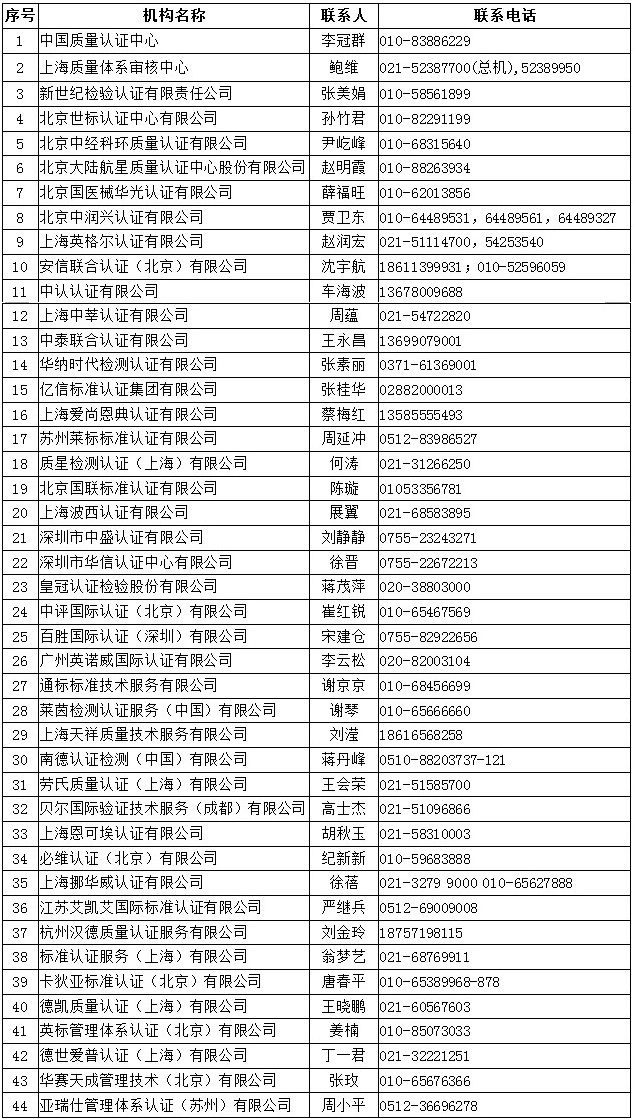
三�����、中國境內(nèi)具有口罩等防疫用品CE認證能力的認證機構(gòu)名錄

四�����、中國境內(nèi)可以開展醫(yī)療器械管理體系(ISO13485)認證的機構(gòu)名錄
標簽:醫(yī)療器械注冊�����、醫(yī)療器械CE認證、醫(yī)療器械經(jīng)營備案