醫(yī)療器械臨床試驗(yàn)研究者文件夾(ISF)該如何管理����?
發(fā)布日期:2019-07-09 23:30瀏覽次數(shù):25317次
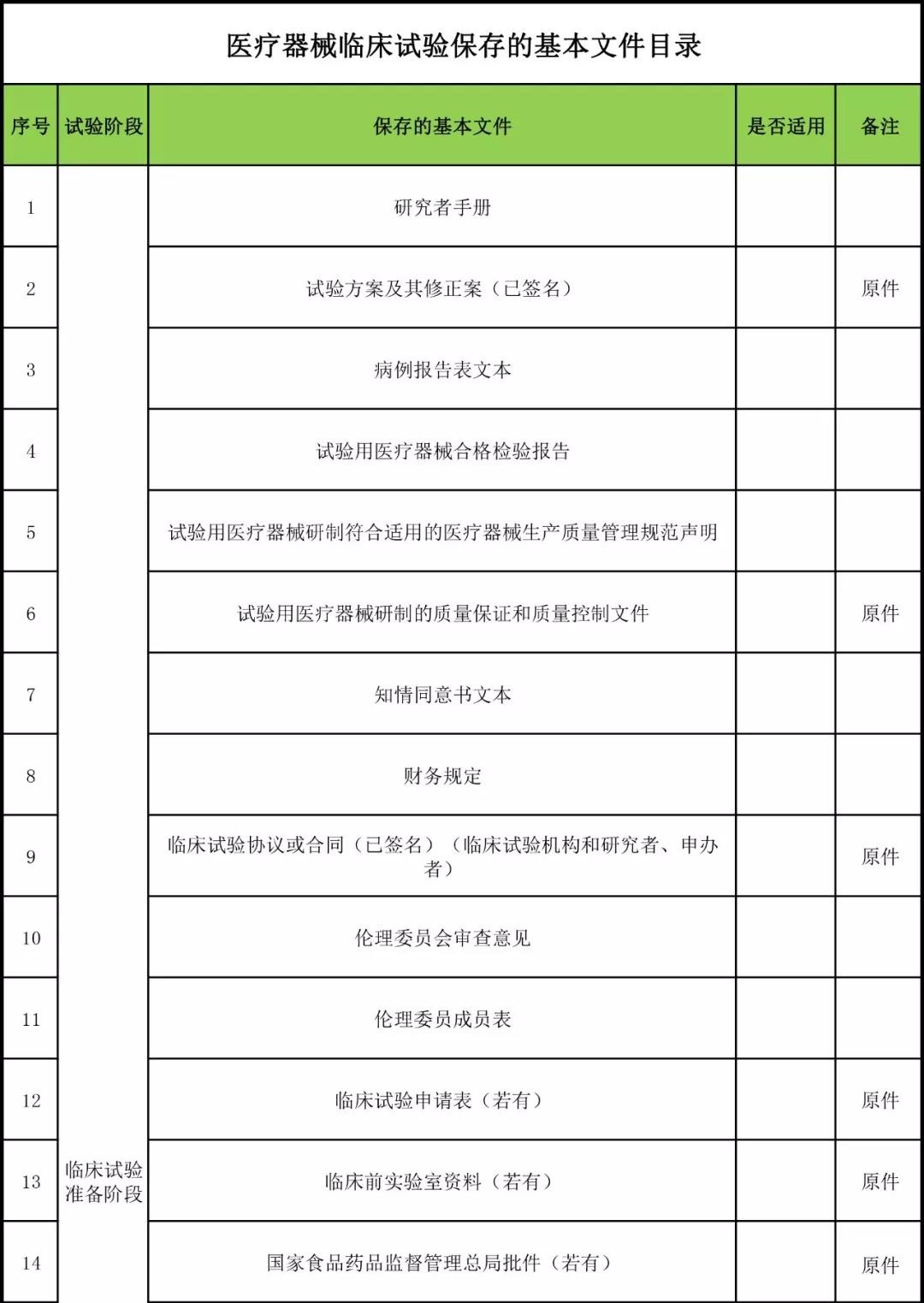
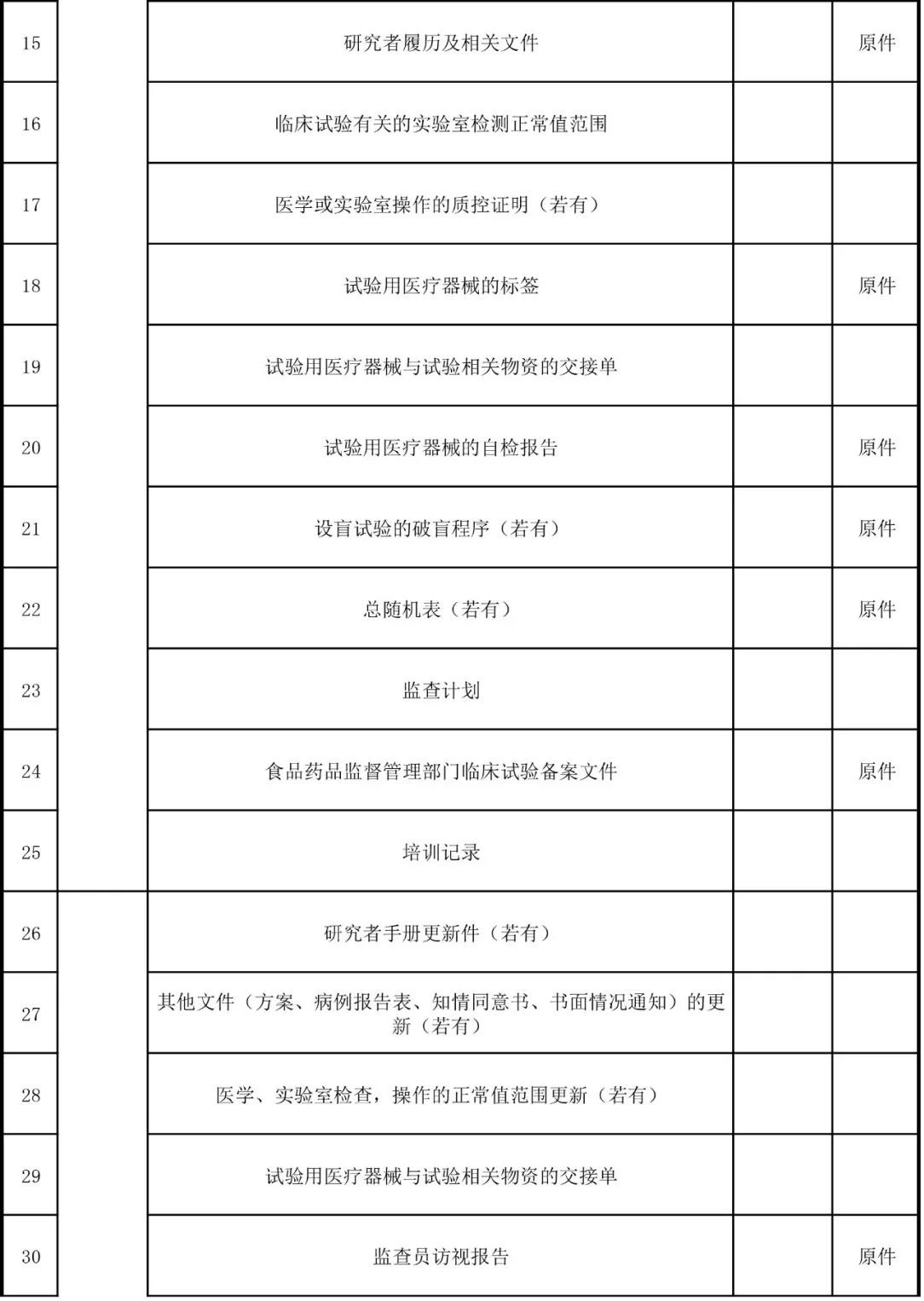
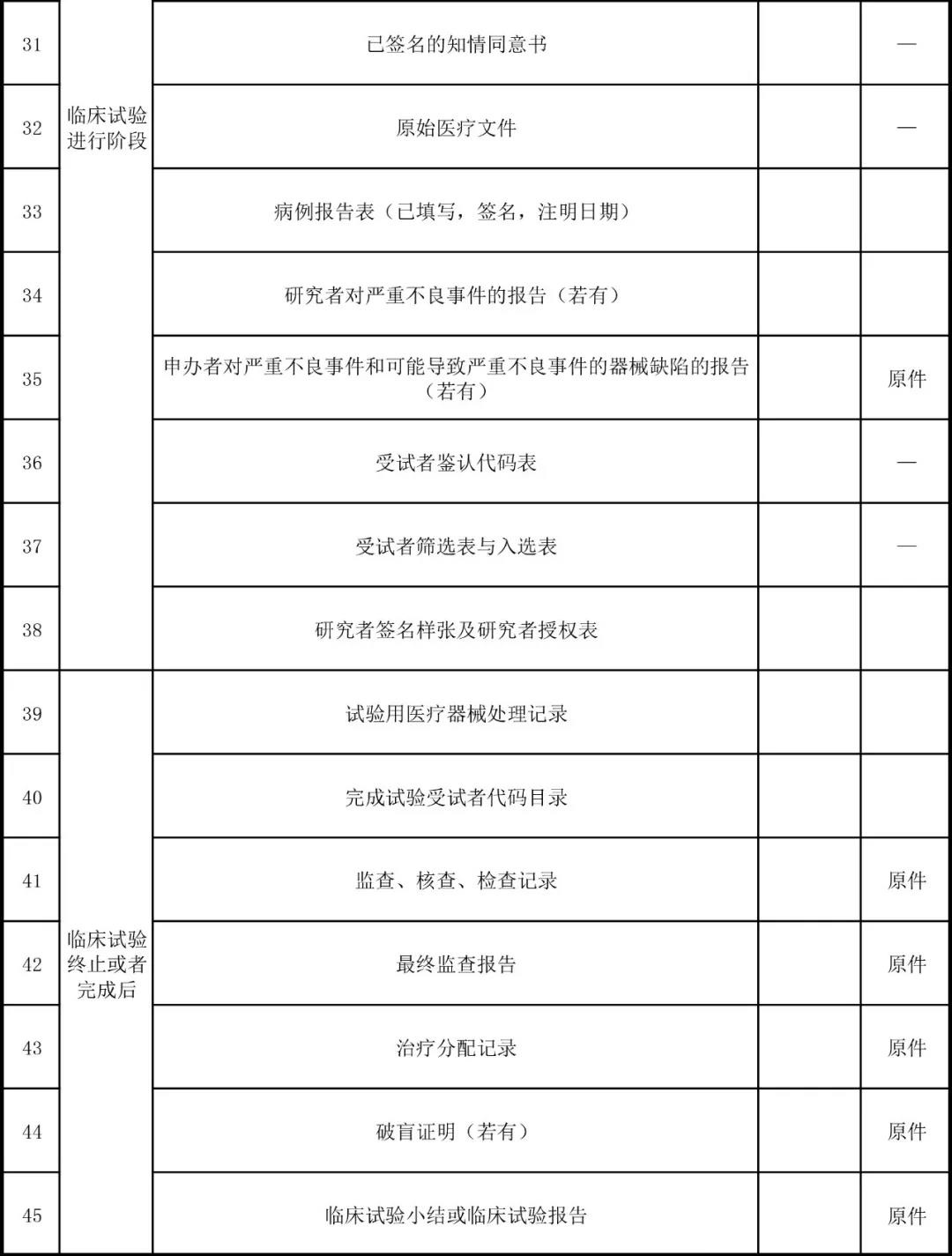
研究者文件夾應(yīng)該包括試驗(yàn)方案、研究者手冊(cè)���、CRF��、ICF���、篩入選表、受試者鑒認(rèn)代碼表�、器械發(fā)放回收記錄、器械的說明書以及檢驗(yàn)報(bào)告���。
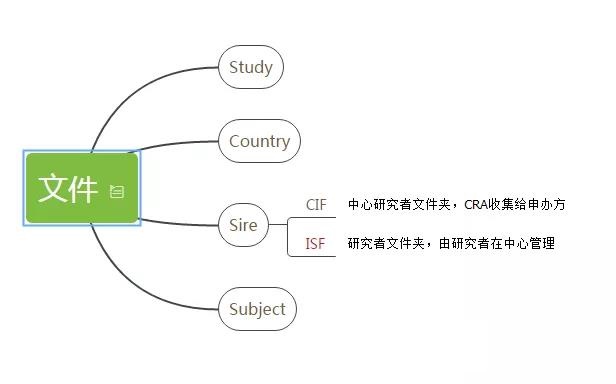
臨床圈的朋友們都知道����,沒有記錄就沒有發(fā)生�����,而對(duì)于一項(xiàng)醫(yī)療器械臨床試驗(yàn)來說,需要記錄的內(nèi)容實(shí)在太多��。一般來說�����,我們會(huì)把這么多的文件分門別類�����,比如分為study層面����,country層面,site層面����,subject層面(由宏觀到微觀)�����,我們今天要講的ISF就屬于site level�����。
研究開始前���,為研究者準(zhǔn)備的或者由研究者準(zhǔn)備的含有臨床研究相關(guān)文件的文件夾�。它保存在研究中心�,由研究者更新并在監(jiān)察時(shí)被監(jiān)察員查看。研究者文件夾需按要求保存�。直至研究結(jié)束后一定的時(shí)限。它也被認(rèn)為是研究中心該研究者管理文件夾或者監(jiān)管文件夾��。
注意點(diǎn):研究者應(yīng)保存臨床試驗(yàn)資料至臨床試驗(yàn)終止后10年����。申辦者應(yīng)保存臨床試驗(yàn)資料至試驗(yàn)藥物被批準(zhǔn)上市后10年。