醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)審查指導(dǎo)原則(2022年修訂版) ��,旨在指導(dǎo)注冊(cè)申請(qǐng)人規(guī)范醫(yī)療器械網(wǎng)絡(luò)安全生存周期過(guò)程和準(zhǔn)備醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)申報(bào)資料�,同時(shí)規(guī)范醫(yī)療器械網(wǎng)絡(luò)安全的技術(shù)審評(píng)要求,為醫(yī)療器械軟件���、質(zhì)量管理軟件的體系核查提供參考�����。
醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)審查指導(dǎo)原則(2022年修訂版)
本指導(dǎo)原則旨在指導(dǎo)注冊(cè)申請(qǐng)人規(guī)范醫(yī)療器械網(wǎng)絡(luò)安全生存周期過(guò)程和準(zhǔn)備醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)申報(bào)資料��,同時(shí)規(guī)范醫(yī)療器械網(wǎng)絡(luò)安全的技術(shù)審評(píng)要求�,為醫(yī)療器械軟件、質(zhì)量管理軟件的體系核查提供參考�����。
本指導(dǎo)原則是對(duì)醫(yī)療器械網(wǎng)絡(luò)安全的一般要求�����,注冊(cè)申請(qǐng)人需根據(jù)產(chǎn)品特性和風(fēng)險(xiǎn)程度確定本指導(dǎo)原則具體內(nèi)容的適用性�����,若不適用詳述理由�。注冊(cè)申請(qǐng)人也可采用其他滿足法規(guī)要求的替代方法,但需提供詳盡的研究資料���。
本指導(dǎo)原則是在現(xiàn)行法規(guī)�����、強(qiáng)制性標(biāo)準(zhǔn)體系以及當(dāng)前科技能力���、認(rèn)知水平下制定的�����,隨著法規(guī)��、強(qiáng)制性標(biāo)準(zhǔn)體系的不斷完善以及科技能力����、認(rèn)知水平的不斷發(fā)展�����,本指導(dǎo)原則相關(guān)內(nèi)容也將適時(shí)調(diào)整���。
本指導(dǎo)原則作為注冊(cè)申請(qǐng)人、審評(píng)人員和檢查人員的指導(dǎo)性文件����,不包括審評(píng)審批所涉及的行政事項(xiàng)���,亦不作為法規(guī)強(qiáng)制執(zhí)行,應(yīng)在符合法規(guī)要求的前提下使用本指導(dǎo)原則��。
本指導(dǎo)原則是數(shù)字醫(yī)療(Digital Health)指導(dǎo)原則體系的重要組成部分���,亦是醫(yī)療器械軟件指導(dǎo)原則的補(bǔ)充���,采用和遵循醫(yī)療器械軟件、獨(dú)立軟件生產(chǎn)質(zhì)量現(xiàn)場(chǎng)檢查等相關(guān)指導(dǎo)原則的概念和要求���。
本指導(dǎo)原則是醫(yī)療器械網(wǎng)絡(luò)安全的通用指導(dǎo)原則����,其他涉及網(wǎng)絡(luò)安全的醫(yī)療器械產(chǎn)品指導(dǎo)原則可在本指導(dǎo)原則基礎(chǔ)上進(jìn)行有針對(duì)性的調(diào)整���、修改和完善����。
一���、適用范圍
本指導(dǎo)原則適用于醫(yī)療器械網(wǎng)絡(luò)安全的注冊(cè)申報(bào)�����,包括具備電子數(shù)據(jù)交換�、遠(yuǎn)程訪問(wèn)與控制、用戶訪問(wèn)三種功能當(dāng)中一種及以上功能的第二�����、三類獨(dú)立軟件和含有軟件組件的醫(yī)療器械(包括體外診斷醫(yī)療器械)��;適用于自研軟件�、現(xiàn)成軟件的注冊(cè)申報(bào)。
其中�����,網(wǎng)絡(luò)包括無(wú)線�����、有線網(wǎng)絡(luò)�����,電子數(shù)據(jù)交換包括基于網(wǎng)絡(luò)���、存儲(chǔ)媒介的單向��、雙向數(shù)據(jù)傳輸���,遠(yuǎn)程訪問(wèn)與控制包括基于網(wǎng)絡(luò)的實(shí)時(shí)、非實(shí)時(shí)的訪問(wèn)與控制����,用戶(如醫(yī)務(wù)人員、患者��、維護(hù)人員等)訪問(wèn)包括基于軟件用戶界面����、電子接口的人機(jī)交互方式。
本指導(dǎo)原則也可用作醫(yī)療器械軟件���、質(zhì)量管理軟件的體系核查參考����。
二�����、主要概念
(一)醫(yī)療器械網(wǎng)絡(luò)安全
醫(yī)療器械網(wǎng)絡(luò)安全是指保護(hù)醫(yī)療器械產(chǎn)品自身和相關(guān)數(shù)據(jù)不受未授權(quán)活動(dòng)影響的狀態(tài),其保密性(Confidentiality)�����、完整性(Integrity)�、可得性(Availability)[1]相關(guān)風(fēng)險(xiǎn)在全生命周期均處于可接受水平[2]。
其中�,保密性是指信息不被未授權(quán)實(shí)體(含產(chǎn)品、服務(wù)��、個(gè)人�����、組織)獲得或知悉的特性�����,即醫(yī)療器械產(chǎn)品自身和相關(guān)數(shù)據(jù)僅可由授權(quán)用戶在授權(quán)時(shí)間以授權(quán)方式進(jìn)行訪問(wèn)和使用����。完整性是指信息的創(chuàng)建、傳輸��、存儲(chǔ)、顯示未以非授權(quán)方式進(jìn)行更改(含刪除���、添加)的特性,即醫(yī)療器械相關(guān)數(shù)據(jù)是準(zhǔn)確和完整的����,且未被篡改?�?傻眯允侵感畔⒖筛鶕?jù)授權(quán)實(shí)體要求進(jìn)行訪問(wèn)和使用的特性��,即醫(yī)療器械產(chǎn)品自身和相關(guān)數(shù)據(jù)能以預(yù)期方式適時(shí)進(jìn)行訪問(wèn)和使用���。
除保密性����、完整性���、可得性三個(gè)基本特性外����,醫(yī)療器械網(wǎng)絡(luò)安全還包括真實(shí)性(Authenticity)����、抗抵賴性(Non-Repudiation)����、可核查性(Accountability)����、可靠性(Reliability)等特性。其中���,真實(shí)性是指實(shí)體符合其所聲稱的特性�,抗抵賴性是指實(shí)體可證明所聲稱事件或活動(dòng)的發(fā)生及其發(fā)起實(shí)體的特性�����,可核查性是指實(shí)體的活動(dòng)及結(jié)果可被追溯的特性�,可靠性是指實(shí)體的活動(dòng)及結(jié)果與預(yù)期保持一致的特性。
保密性�、完整性、可得性等網(wǎng)絡(luò)安全特性通常是相互制約的關(guān)系�,在同等條件下,某一特性的能力提升可能會(huì)使得另一特性或多個(gè)特性的能力下降�����,如可得性的提升可能會(huì)降低保密性和完整性,因此需要基于產(chǎn)品特性進(jìn)行平衡兼顧�����。注冊(cè)申請(qǐng)人需結(jié)合醫(yī)療器械的預(yù)期用途�����、使用場(chǎng)景�����、核心功能進(jìn)行綜合考量���,從而確定醫(yī)療器械網(wǎng)絡(luò)安全特性的具體要求。
此外�����,盡管信息安全�、網(wǎng)絡(luò)安全、數(shù)據(jù)安全的定義和范圍各有側(cè)重���,既有聯(lián)系又有區(qū)別��,不盡相同����,但本指導(dǎo)原則從醫(yī)療器械安全有效性評(píng)價(jià)角度出發(fā)對(duì)三者不做嚴(yán)格區(qū)分,統(tǒng)一采用網(wǎng)絡(luò)安全進(jìn)行表述��,即從網(wǎng)絡(luò)安全角度綜合考慮醫(yī)療器械的信息安全和數(shù)據(jù)安全�����。
(二)醫(yī)療器械相關(guān)數(shù)據(jù)
醫(yī)療器械相關(guān)數(shù)據(jù)可分為醫(yī)療數(shù)據(jù)和設(shè)備數(shù)據(jù)���。
醫(yī)療數(shù)據(jù)是指醫(yī)療器械所產(chǎn)生的����、使用的與醫(yī)療活動(dòng)相關(guān)的數(shù)據(jù)(含日志)����,從個(gè)人信息保護(hù)角度又可分為敏感醫(yī)療數(shù)據(jù)、非敏感醫(yī)療數(shù)據(jù)�,其中敏感醫(yī)療數(shù)據(jù)是指含有個(gè)人信息的醫(yī)療數(shù)據(jù)[3],反之即為非敏感醫(yī)療數(shù)據(jù)����。個(gè)人信息是指以電子或者其他方式記錄的能夠單獨(dú)或與其他信息結(jié)合識(shí)別自然人個(gè)人身份的各種信息�,如自然人的姓名����、出生日期、身份證件號(hào)碼���、個(gè)人生物識(shí)別信息(含容貌信息)���、住址、電話號(hào)碼等���。
設(shè)備數(shù)據(jù)是指記錄醫(yī)療器械運(yùn)行狀況的數(shù)據(jù)(含日志)���,用于監(jiān)視、控制醫(yī)療器械運(yùn)行或者醫(yī)療器械的維護(hù)與升級(jí)��,不得含有個(gè)人信息。
注冊(cè)申請(qǐng)人需基于醫(yī)療器械相關(guān)數(shù)據(jù)的類型��、功能、用途����,結(jié)合網(wǎng)絡(luò)安全特性考慮醫(yī)療器械網(wǎng)絡(luò)安全要求�。同時(shí)��,保證敏感醫(yī)療數(shù)據(jù)所含個(gè)人信息免于泄露���、濫用和篡改,以及醫(yī)療數(shù)據(jù)和設(shè)備數(shù)據(jù)的有效隔離(如訪問(wèn)權(quán)限控制等方法)�。
(三)醫(yī)療器械電子接口
本指導(dǎo)原則所述醫(yī)療器械電子接口(含硬件接口���、軟件接口)包括網(wǎng)絡(luò)接口����、電子數(shù)據(jù)交換接口����,若無(wú)明示均指外部接口���,分體式醫(yī)療器械各獨(dú)立部分的內(nèi)部接口視為外部接口��,如服務(wù)器與客戶端�����、主機(jī)與從機(jī)的內(nèi)部接口����。
1.網(wǎng)絡(luò)接口
網(wǎng)絡(luò)接口是指基于網(wǎng)絡(luò)的電子接口����。醫(yī)療器械可通過(guò)網(wǎng)絡(luò)接口(含轉(zhuǎn)接接口)進(jìn)行電子數(shù)據(jù)交換或遠(yuǎn)程訪問(wèn)與控制,此時(shí)需考慮網(wǎng)絡(luò)的技術(shù)特征要求�����,包括但不限于網(wǎng)絡(luò)形式(有線����、無(wú)線)、網(wǎng)絡(luò)類型(如廣域網(wǎng)�����、局域網(wǎng)、個(gè)域網(wǎng))��、接口形式(如電口��、光口)、數(shù)據(jù)接口(此時(shí)即數(shù)據(jù)協(xié)議��,含標(biāo)準(zhǔn)協(xié)議、私有協(xié)議)、遠(yuǎn)程訪問(wèn)與控制方式(實(shí)時(shí)�����、非實(shí)時(shí))、性能指標(biāo)(如端口���、傳輸速率�����、帶寬)等����。
無(wú)線網(wǎng)絡(luò)包括Wi-Fi(IEEE 802.11)�����、藍(lán)牙(IEEE 802.15)�����、射頻�、紅外、4G/5G等形式�,其中醫(yī)用無(wú)線專用設(shè)備(即未采用通用無(wú)線通信技術(shù)的醫(yī)療器械)應(yīng)符合中國(guó)無(wú)線電管理相關(guān)規(guī)定����。標(biāo)準(zhǔn)協(xié)議即業(yè)內(nèi)公認(rèn)標(biāo)準(zhǔn)所規(guī)范的數(shù)據(jù)傳輸協(xié)議,如DICOM�����、HL7等�����,需考慮其定制化功能的兼容性問(wèn)題���;私有協(xié)議需考慮兼容性問(wèn)題�。遠(yuǎn)程訪問(wèn)與控制亦包括操作系統(tǒng)軟件所提供的遠(yuǎn)程會(huì)話或遠(yuǎn)程桌面功能�����。
2.電子數(shù)據(jù)交換接口
電子數(shù)據(jù)交換接口是指基于非網(wǎng)絡(luò)的電子接口。醫(yī)療器械可通過(guò)非網(wǎng)絡(luò)接口的其他電子接口(如串口�、并口����、USB口、視頻接口��、音頻接口��,含調(diào)試接口�、轉(zhuǎn)接接口)或存儲(chǔ)媒介(如光盤���、移動(dòng)硬盤���、U盤)進(jìn)行電子數(shù)據(jù)交換��。此時(shí)需考慮其他電子接口或數(shù)據(jù)存儲(chǔ)的技術(shù)特征要求���。
其他電子接口可參照網(wǎng)絡(luò)接口明確其技術(shù)特征要求�����。數(shù)據(jù)存儲(chǔ)的技術(shù)特征要求包括但不限于存儲(chǔ)媒介形式����、數(shù)據(jù)接口(此時(shí)即文件存儲(chǔ)格式�,含標(biāo)準(zhǔn)格式��、私有格式)��、數(shù)據(jù)壓縮方式(有損�����、無(wú)損)�����、性能指標(biāo)(如傳輸速率�����、容量)等�����。標(biāo)準(zhǔn)格式即業(yè)內(nèi)公認(rèn)標(biāo)準(zhǔn)所規(guī)范的文件存儲(chǔ)格式���,如JPEG、PNG等���,需考慮其文件格式完整性問(wèn)題;私有格式需考慮兼容性問(wèn)題�����。
注冊(cè)申請(qǐng)人需結(jié)合醫(yī)療器械電子接口的類型�、方式、技術(shù)特征���,基于網(wǎng)絡(luò)安全特性考慮其網(wǎng)絡(luò)安全的具體要求。
(四)醫(yī)療器械網(wǎng)絡(luò)安全能力
考慮到預(yù)期用途�、使用場(chǎng)景的限制�����,醫(yī)療器械對(duì)于網(wǎng)絡(luò)安全威脅應(yīng)具備必要的識(shí)別�����、保護(hù)能力和適當(dāng)?shù)奶綔y(cè)�、響應(yīng)���、恢復(fù)能力。
本指導(dǎo)原則所述醫(yī)療器械網(wǎng)絡(luò)安全能力包括:
1.自動(dòng)注銷(ALOF):產(chǎn)品在無(wú)人值守期間阻止非授權(quán)用戶訪問(wèn)和使用的能力。
2.審核(AUDT):產(chǎn)品提供用戶活動(dòng)可被審核的能力���。
3.授權(quán)(AUTH):產(chǎn)品確定用戶已獲授權(quán)的能力�����。
4.節(jié)點(diǎn)鑒別(NAUT):產(chǎn)品鑒別網(wǎng)絡(luò)節(jié)點(diǎn)的能力。
5.人員鑒別(PAUT):產(chǎn)品鑒別授權(quán)用戶的能力���。
6.連通性(CONN):產(chǎn)品保證連通網(wǎng)絡(luò)安全可控的能力�。
7.物理防護(hù)(PLOK):產(chǎn)品提供防止非授權(quán)用戶訪問(wèn)和使用的物理防護(hù)措施的能力���。
8.系統(tǒng)加固(SAHD):產(chǎn)品通過(guò)固化措施對(duì)網(wǎng)絡(luò)攻擊和惡意軟件的抵御能力���。
9.數(shù)據(jù)去標(biāo)識(shí)化與匿名化(DIDT):產(chǎn)品直接去除、匿名化數(shù)據(jù)所含個(gè)人信息的能力��。
10.數(shù)據(jù)完整性與真實(shí)性(IGAU):產(chǎn)品確保數(shù)據(jù)未以非授權(quán)方式更改且來(lái)自創(chuàng)建者或提供者的能力�����。
11.數(shù)據(jù)備份與災(zāi)難恢復(fù)(DTBK):產(chǎn)品的數(shù)據(jù)��、硬件或軟件受到損壞或破壞后恢復(fù)的能力�����。
12.數(shù)據(jù)存儲(chǔ)保密性與完整性(STCF):產(chǎn)品確保未授權(quán)訪問(wèn)不會(huì)損壞存儲(chǔ)媒介所存數(shù)據(jù)保密性和完整性的能力��。
13.數(shù)據(jù)傳輸保密性(TXCF):產(chǎn)品確保數(shù)據(jù)傳輸保密性的能力���。
14.數(shù)據(jù)傳輸完整性(TXIG):產(chǎn)品確保數(shù)據(jù)傳輸完整性的能力�。
15.網(wǎng)絡(luò)安全補(bǔ)丁升級(jí)(CSUP):授權(quán)用戶安裝/升級(jí)產(chǎn)品網(wǎng)絡(luò)安全補(bǔ)丁的能力���。
16.現(xiàn)成軟件清單(SBOM):產(chǎn)品為用戶提供全部現(xiàn)成軟件清單的能力���。
17.現(xiàn)成軟件維護(hù)(RDMP):產(chǎn)品在全生命周期中對(duì)現(xiàn)成軟件提供網(wǎng)絡(luò)安全維護(hù)的能力。
18.網(wǎng)絡(luò)安全使用指導(dǎo)(SGUD):產(chǎn)品為用戶提供網(wǎng)絡(luò)安全使用指導(dǎo)的能力�。
19.網(wǎng)絡(luò)安全特征配置(CNFS):產(chǎn)品根據(jù)用戶需求配置網(wǎng)絡(luò)安全特征的能力。
20.緊急訪問(wèn)(EMRG):產(chǎn)品在預(yù)期緊急情況下允許用戶訪問(wèn)和使用的能力����。
21.遠(yuǎn)程訪問(wèn)與控制(RMOT):產(chǎn)品確保用戶遠(yuǎn)程訪問(wèn)與控制(含遠(yuǎn)程維護(hù)與升級(jí))的網(wǎng)絡(luò)安全的能力。
22.惡意軟件探測(cè)與防護(hù)(MLDP):產(chǎn)品有效探測(cè)���、阻止惡意軟件的能力�。
注冊(cè)申請(qǐng)人需根據(jù)醫(yī)療器械的產(chǎn)品特性分析上述網(wǎng)絡(luò)安全能力的適用性��。若適用����,明確網(wǎng)絡(luò)安全能力的實(shí)現(xiàn)方式����,可通過(guò)產(chǎn)品自身功能實(shí)現(xiàn)�����,亦可通過(guò)必備軟件��、外部軟件環(huán)境等外部措施實(shí)現(xiàn)���。同時(shí)�����,根據(jù)產(chǎn)品風(fēng)險(xiǎn)水平明確網(wǎng)絡(luò)安全能力的強(qiáng)弱程度��,例如:用戶訪問(wèn)控制可采用用戶名和口令方式����,其中口令強(qiáng)度可采用不同強(qiáng)度設(shè)置或采用動(dòng)態(tài)口令��,亦可采用生物識(shí)別技術(shù)����,通常情況下醫(yī)療器械的風(fēng)險(xiǎn)水平越高則其用戶訪問(wèn)控制要求越嚴(yán)格。反之�,若不適用詳述理由并予以記錄。
值得注意的是�����,對(duì)于特定醫(yī)療器械產(chǎn)品���,上述各項(xiàng)網(wǎng)絡(luò)安全能力可能不足以保證其網(wǎng)絡(luò)安全�,需結(jié)合產(chǎn)品具體情況補(bǔ)充其他網(wǎng)絡(luò)安全能力要求�。
(五)網(wǎng)絡(luò)安全驗(yàn)證與確認(rèn)
網(wǎng)絡(luò)安全驗(yàn)證與確認(rèn)作為軟件驗(yàn)證與確認(rèn)的重要組成部分,需在軟件驗(yàn)證與確認(rèn)的框架下��,結(jié)合產(chǎn)品網(wǎng)絡(luò)安全特性開(kāi)展相關(guān)質(zhì)控工作���,如源代碼安全審核��、威脅建模�、漏洞掃描�����、滲透測(cè)試����、模糊測(cè)試等����。軟件驗(yàn)證與確認(rèn)相關(guān)要求詳見(jiàn)醫(yī)療器械軟件指導(dǎo)原則第二章��。
注冊(cè)申請(qǐng)人需針對(duì)不同類型網(wǎng)絡(luò)威脅�����,采用相應(yīng)技術(shù)手段來(lái)保證醫(yī)療器械的網(wǎng)絡(luò)安全���。例如:針對(duì)讀取攻擊����、操作攻擊�、欺騙攻擊、泛洪攻擊���、重定向�����、勒索攻擊等網(wǎng)絡(luò)威脅���,可采用用戶訪問(wèn)控制、端口與服務(wù)關(guān)閉��、加密�����、數(shù)字簽名����、標(biāo)準(zhǔn)協(xié)議、校驗(yàn)�����、防火墻�����、入侵檢測(cè)����、惡意代碼防護(hù)、防護(hù)規(guī)則配置等方法與技術(shù)來(lái)保證產(chǎn)品的網(wǎng)絡(luò)安全�����。
(六)網(wǎng)絡(luò)安全可追溯性分析
網(wǎng)絡(luò)安全可追溯性分析作為網(wǎng)絡(luò)安全驗(yàn)證與確認(rèn)的重要活動(dòng)之一,是指追蹤網(wǎng)絡(luò)安全需求��、網(wǎng)絡(luò)安全設(shè)計(jì)�����、源代碼���、網(wǎng)絡(luò)安全測(cè)試��、網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理之間的關(guān)系���,分析已識(shí)別關(guān)系的正確性、一致性��、完整性��、準(zhǔn)確性��。
醫(yī)療器械網(wǎng)絡(luò)安全生存周期過(guò)程均應(yīng)開(kāi)展網(wǎng)絡(luò)安全可追溯性分析活動(dòng)���,具體要求可參照軟件可追溯性分析活動(dòng)要求����,詳見(jiàn)醫(yī)療器械軟件指導(dǎo)原則第二章。
(七)網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)
醫(yī)療器械設(shè)計(jì)開(kāi)發(fā)只能針對(duì)已知網(wǎng)絡(luò)安全漏洞采取相應(yīng)風(fēng)險(xiǎn)控制措施�����,上市后仍會(huì)面臨潛在未知的網(wǎng)絡(luò)安全漏洞引發(fā)的網(wǎng)絡(luò)安全事件的威脅���,可能造成醫(yī)療器械無(wú)法訪問(wèn)和使用、醫(yī)療數(shù)據(jù)發(fā)生泄露或遭到篡改�����,進(jìn)而可能導(dǎo)致患者受到傷害或死亡以及隱私被侵犯�����。同時(shí)�,醫(yī)療器械網(wǎng)絡(luò)安全事件具有影響因素多、涉及面廣����、擴(kuò)散性強(qiáng)和突發(fā)性高等特點(diǎn),對(duì)于醫(yī)療器械上市后監(jiān)測(cè)要求相對(duì)較高。因此����,注冊(cè)申請(qǐng)人需基于相關(guān)標(biāo)準(zhǔn)和技術(shù)報(bào)告建立網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)機(jī)制,保證醫(yī)療器械的安全有效性并保護(hù)患者隱私��。
應(yīng)制定網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)預(yù)案����,涵蓋現(xiàn)成軟件要求,明確計(jì)劃與準(zhǔn)備�、探測(cè)與報(bào)告、評(píng)估與決策����、應(yīng)急響應(yīng)實(shí)施、總結(jié)與改進(jìn)等階段的任務(wù)和要求���。建立網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)團(tuán)隊(duì)����,根據(jù)工作職能形成管理���、規(guī)劃�、監(jiān)測(cè)、響應(yīng)���、實(shí)施�、分析等工作小組��,必要時(shí)可邀請(qǐng)外部網(wǎng)絡(luò)安全專家成立專家小組����。
根據(jù)網(wǎng)絡(luò)安全事件的嚴(yán)重程度、緊迫程度��、廣泛程度等因素進(jìn)行分類分級(jí)管理�����,結(jié)合產(chǎn)品風(fēng)險(xiǎn)級(jí)別��,按照風(fēng)險(xiǎn)管理要求開(kāi)展應(yīng)急響應(yīng)措施的驗(yàn)證工作并予以記錄���,在事件發(fā)生期間及時(shí)告知用戶應(yīng)對(duì)措施。若適用���,按照醫(yī)療器械不良事件�、召回相關(guān)法規(guī)要求處理;必要時(shí)�����,向國(guó)家網(wǎng)絡(luò)安全主管部門報(bào)告����。
(八)醫(yī)療器械網(wǎng)絡(luò)安全更新
1.網(wǎng)絡(luò)安全更新
醫(yī)療器械網(wǎng)絡(luò)安全更新從內(nèi)容上可分為功能更新、補(bǔ)丁更新�,類似于增強(qiáng)類軟件更新、糾正類軟件更新�����。根據(jù)其對(duì)醫(yī)療器械安全性和有效性的影響程度分為以下兩類:
(1)重大網(wǎng)絡(luò)安全更新:影響到醫(yī)療器械的安全性或有效性的網(wǎng)絡(luò)安全更新���,即重大網(wǎng)絡(luò)安全功能更新��,應(yīng)申請(qǐng)變更注冊(cè)��。
(2)輕微網(wǎng)絡(luò)安全更新:不影響醫(yī)療器械的安全性與有效性的網(wǎng)絡(luò)安全更新�,包括輕微網(wǎng)絡(luò)安全功能更新���、網(wǎng)絡(luò)安全補(bǔ)丁更新�。輕微網(wǎng)絡(luò)安全更新通過(guò)質(zhì)量管理體系進(jìn)行控制,無(wú)需申請(qǐng)變更注冊(cè)����,待下次變更注冊(cè)時(shí)提交相應(yīng)注冊(cè)申報(bào)資料。
此外�,涉及召回的網(wǎng)絡(luò)安全更新,無(wú)論功能更新還是補(bǔ)丁更新均屬于重大網(wǎng)絡(luò)安全更新��,按照醫(yī)療器械召回相關(guān)法規(guī)要求處理���,不屬于本指導(dǎo)原則討論范疇���。
網(wǎng)絡(luò)安全更新同樣遵循風(fēng)險(xiǎn)從高原則,即同時(shí)發(fā)生重大和輕微網(wǎng)絡(luò)安全更新按重大網(wǎng)絡(luò)安全更新處理�����。同時(shí)�,軟件版本命名規(guī)則應(yīng)涵蓋網(wǎng)絡(luò)安全更新情況�����,區(qū)分重大和輕微網(wǎng)絡(luò)安全更新�。
2.重大網(wǎng)絡(luò)安全更新判定原則
網(wǎng)絡(luò)安全功能更新若影響到醫(yī)療器械的預(yù)期用途�����、使用場(chǎng)景或核心功能原則上均屬于重大網(wǎng)絡(luò)安全更新�,包括但不限于:產(chǎn)品預(yù)期運(yùn)行的網(wǎng)絡(luò)環(huán)境發(fā)生改變�,如由封閉網(wǎng)絡(luò)環(huán)境變?yōu)殚_(kāi)放網(wǎng)絡(luò)環(huán)境、局域網(wǎng)變?yōu)閺V域網(wǎng)��、有線網(wǎng)絡(luò)變?yōu)闊o(wú)線網(wǎng)絡(luò)�����;產(chǎn)品預(yù)期使用的電子接口發(fā)生改變���,如接口形式由網(wǎng)口變?yōu)閁SB口�、接口類型由少變多�、接口功能由電子數(shù)據(jù)交換擴(kuò)至遠(yuǎn)程控制;產(chǎn)品網(wǎng)絡(luò)安全能力發(fā)生實(shí)質(zhì)性改變��,如自動(dòng)注銷能力由操作系統(tǒng)自帶功能實(shí)現(xiàn)改為產(chǎn)品自身功能實(shí)現(xiàn)��、物理防護(hù)能力由有變無(wú)等��。
除非影響到醫(yī)療器械的安全性或有效性���,以下網(wǎng)絡(luò)安全功能更新和網(wǎng)絡(luò)安全補(bǔ)丁更新通常視為輕微網(wǎng)絡(luò)安全更新:產(chǎn)品預(yù)期運(yùn)行的網(wǎng)絡(luò)環(huán)境數(shù)據(jù)傳輸效率單純提高���,預(yù)期使用的電子接口原有功能單純優(yōu)化�����、傳輸效率單純提高�,產(chǎn)品網(wǎng)絡(luò)安全能力發(fā)生非實(shí)質(zhì)性改變��;醫(yī)療器械軟件��、必備軟件��、外部軟件環(huán)境的網(wǎng)絡(luò)安全補(bǔ)丁更新�。其中,必備軟件是指醫(yī)療器械軟件正常運(yùn)行所必需的其他醫(yī)療器械軟件及醫(yī)用中間件����,外部軟件環(huán)境是指醫(yī)療器械軟件正常運(yùn)行所必需的系統(tǒng)軟件��、通用應(yīng)用軟件�、通用中間件、支持軟件���,詳見(jiàn)醫(yī)療器械軟件指導(dǎo)原則��。
三�����、基本原則
(一)網(wǎng)絡(luò)安全定位
隨著網(wǎng)絡(luò)技術(shù)的發(fā)展��,越來(lái)越多的醫(yī)療器械具備網(wǎng)絡(luò)連接功能以進(jìn)行電子數(shù)據(jù)交換或遠(yuǎn)程訪問(wèn)與控制���,在提高醫(yī)療服務(wù)質(zhì)量與效率的同時(shí)也面臨著網(wǎng)絡(luò)攻擊的威脅��。醫(yī)療器械網(wǎng)絡(luò)安全出現(xiàn)問(wèn)題不僅可能會(huì)侵犯患者隱私���,而且可能會(huì)產(chǎn)生醫(yī)療器械非預(yù)期運(yùn)行的風(fēng)險(xiǎn),導(dǎo)致患者或用戶受到傷害或死亡�����。因此�����,醫(yī)療器械網(wǎng)絡(luò)安全是醫(yī)療器械安全性和有效性的重要組成部分之一。
信息共享是保障醫(yī)療器械網(wǎng)絡(luò)安全的基本原則[4]�。及時(shí)獲得網(wǎng)絡(luò)安全漏洞、事件等相關(guān)信息有助于識(shí)別�����、評(píng)估和應(yīng)對(duì)網(wǎng)絡(luò)安全風(fēng)險(xiǎn)����,保證醫(yī)療器械的安全有效性以及醫(yī)療活動(dòng)的業(yè)務(wù)持續(xù)性,因此��,鼓勵(lì)所有利益相關(guān)方在醫(yī)療器械全生命周期中主動(dòng)積極共享網(wǎng)絡(luò)安全相關(guān)信息���。注冊(cè)申請(qǐng)人需充分利用網(wǎng)絡(luò)安全漏洞披露機(jī)制加強(qiáng)醫(yī)療器械網(wǎng)絡(luò)安全的設(shè)計(jì)開(kāi)發(fā)和上市后監(jiān)測(cè)�����,如基于國(guó)家互聯(lián)網(wǎng)應(yīng)急中心(CNCERT/CC����,www.cert.org.cn)的國(guó)家信息安全漏洞共享平臺(tái)(CNVD�����,www.cnvd.org.cn)����,或其互認(rèn)的國(guó)際信息安全漏洞庫(kù)所披露的漏洞信息,定期開(kāi)展網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理工作��。
醫(yī)療器械網(wǎng)絡(luò)安全需要注冊(cè)申請(qǐng)人��、用戶�、信息技術(shù)服務(wù)商等利益相關(guān)者的共同努力和通力合作方能得以保障。雖然醫(yī)療器械在使用過(guò)程中常與非預(yù)期的設(shè)備或系統(tǒng)相連���,使得注冊(cè)申請(qǐng)人在保證醫(yī)療器械網(wǎng)絡(luò)安全方面存在諸多困難����,但這不意味注冊(cè)申請(qǐng)人可以免除醫(yī)療器械網(wǎng)絡(luò)安全相關(guān)責(zé)任��。注冊(cè)申請(qǐng)人需保證醫(yī)療器械產(chǎn)品自身的網(wǎng)絡(luò)安全��,明確預(yù)期的網(wǎng)絡(luò)環(huán)境和電子接口要求��,持續(xù)監(jiān)測(cè)�����、評(píng)估、應(yīng)對(duì)����、分享網(wǎng)絡(luò)安全相關(guān)風(fēng)險(xiǎn),與其他利益相關(guān)者密切合作����,從而保證醫(yī)療器械的安全有效性。
醫(yī)療器械網(wǎng)絡(luò)安全也是網(wǎng)絡(luò)安全國(guó)家戰(zhàn)略的重要組成部分�,因此醫(yī)療器械網(wǎng)絡(luò)安全亦應(yīng)符合網(wǎng)絡(luò)安全相關(guān)法律法規(guī)和部門規(guī)章的要求,如網(wǎng)絡(luò)安全法�、數(shù)據(jù)安全法、個(gè)人信息保護(hù)法以及數(shù)據(jù)出境�、重要數(shù)據(jù)識(shí)別等要求。注冊(cè)申請(qǐng)人應(yīng)持續(xù)跟蹤相關(guān)法律法規(guī)和部門規(guī)章的制修訂情況�����,并滿足相應(yīng)適用要求�����。
網(wǎng)絡(luò)安全新技術(shù)(如人工智能技術(shù))研究處于快速發(fā)展階段����,醫(yī)療器械若采用網(wǎng)絡(luò)安全新技術(shù)來(lái)保證網(wǎng)絡(luò)安全�����,亦需基于新技術(shù)特性,并結(jié)合風(fēng)險(xiǎn)管理開(kāi)展相應(yīng)驗(yàn)證與確認(rèn)工作�。
(二)風(fēng)險(xiǎn)導(dǎo)向
綜合考慮行業(yè)發(fā)展水平和風(fēng)險(xiǎn)分級(jí)管理導(dǎo)向,醫(yī)療器械網(wǎng)絡(luò)安全的風(fēng)險(xiǎn)級(jí)別不同���,其生命周期質(zhì)控要求和注冊(cè)申報(bào)資料要求亦不同����。
雖然網(wǎng)絡(luò)安全風(fēng)險(xiǎn)與軟件風(fēng)險(xiǎn)存在差異���,但是網(wǎng)絡(luò)安全風(fēng)險(xiǎn)作為軟件風(fēng)險(xiǎn)的重要組成部分���,其風(fēng)險(xiǎn)級(jí)別亦可參照軟件采用安全性級(jí)別進(jìn)行表述[5]。在通常情形下�,醫(yī)療器械網(wǎng)絡(luò)安全的安全性級(jí)別與所屬醫(yī)療器械軟件的安全性級(jí)別相同;在特殊情形下�,網(wǎng)絡(luò)安全的安全性級(jí)別可低于軟件的安全性級(jí)別,此時(shí)需詳述理由并按網(wǎng)絡(luò)安全的安全性級(jí)別提交相應(yīng)注冊(cè)申報(bào)資料�����。
醫(yī)療器械網(wǎng)絡(luò)安全風(fēng)險(xiǎn)同樣結(jié)合醫(yī)療器械的預(yù)期用途、使用場(chǎng)景�����、核心功能進(jìn)行綜合判定��,特別是使用場(chǎng)景���。不同使用場(chǎng)景的網(wǎng)絡(luò)環(huán)境不同����,甚至存在巨大差異���,對(duì)于醫(yī)療器械網(wǎng)絡(luò)安全的影響亦不同����,如門診��、手術(shù)�、住院、急救�����、家庭、轉(zhuǎn)運(yùn)���、公共場(chǎng)所等使用場(chǎng)景的網(wǎng)絡(luò)環(huán)境均有所不同�,因此對(duì)于適用于多個(gè)使用場(chǎng)景的醫(yī)療器械����,注冊(cè)申請(qǐng)人需保證醫(yī)療器械在每個(gè)使用場(chǎng)景的網(wǎng)絡(luò)安全�����。
醫(yī)療器械網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理活動(dòng)通常包括:識(shí)別資產(chǎn)(Asset����,對(duì)個(gè)人或組織有價(jià)值的物理和數(shù)字實(shí)體)、威脅(Threat�����,可能導(dǎo)致對(duì)個(gè)人或組織產(chǎn)生損害的非預(yù)期事件發(fā)生的潛在原因)和脆弱性(Vulnerability�����,可能會(huì)被威脅所利用的資產(chǎn)或風(fēng)險(xiǎn)控制措施的弱點(diǎn))��,評(píng)估威脅和脆弱性對(duì)于醫(yī)療器械和患者的影響以及被利用的可能性,確定風(fēng)險(xiǎn)水平并采取充分����、有效、適宜的風(fēng)險(xiǎn)控制措施���,基于風(fēng)險(xiǎn)接受準(zhǔn)則評(píng)估網(wǎng)絡(luò)安全綜合剩余風(fēng)險(xiǎn)�,保證網(wǎng)絡(luò)安全綜合剩余風(fēng)險(xiǎn)均處于可接受水平��。
注冊(cè)申請(qǐng)人可結(jié)合醫(yī)療器械風(fēng)險(xiǎn)管理和網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理相關(guān)標(biāo)準(zhǔn)和技術(shù)報(bào)告的要求�����,開(kāi)展醫(yī)療器械網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理工作��。值得注意的是�,醫(yī)療器械風(fēng)險(xiǎn)管理與網(wǎng)絡(luò)安全風(fēng)險(xiǎn)管理在傳統(tǒng)上存在一定差異,注冊(cè)申請(qǐng)人若無(wú)法對(duì)二者進(jìn)行有效整合����,則需分別獨(dú)立開(kāi)展相應(yīng)風(fēng)險(xiǎn)管理活動(dòng)并予以記錄,同時(shí)考慮不同類型風(fēng)險(xiǎn)控制措施的相互影響問(wèn)題�����。
(三)全生命周期質(zhì)控
與醫(yī)療器械軟件類似,注冊(cè)申請(qǐng)人應(yīng)在醫(yī)療器械全生命周期中持續(xù)關(guān)注網(wǎng)絡(luò)安全問(wèn)題�����,包括上市前����、上市后等階段。
醫(yī)療器械上市前結(jié)合質(zhì)量管理體系要求和醫(yī)療器械產(chǎn)品特性開(kāi)展網(wǎng)絡(luò)安全質(zhì)控工作�,保證醫(yī)療器械的安全有效性;上市后根據(jù)網(wǎng)絡(luò)安全更新情況開(kāi)展更新請(qǐng)求評(píng)估�����、驗(yàn)證與確認(rèn)�����、風(fēng)險(xiǎn)管理��、用戶告知等活動(dòng)�����,持續(xù)保證醫(yī)療器械的安全有效性����。同時(shí),建立網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)過(guò)程��,定期開(kāi)展醫(yī)療器械網(wǎng)絡(luò)安全漏洞風(fēng)險(xiǎn)評(píng)估工作���,根據(jù)網(wǎng)絡(luò)安全漏洞披露相關(guān)要求����,及時(shí)將必要的網(wǎng)絡(luò)安全相關(guān)信息以及應(yīng)對(duì)措施告知用戶��。此外�����,可采用信息安全領(lǐng)域的良好工程實(shí)踐[6]來(lái)完善醫(yī)療器械網(wǎng)絡(luò)安全質(zhì)控工作��,以保證醫(yī)療器械的安全有效性��。
四���、醫(yī)療器械網(wǎng)絡(luò)安全生存周期過(guò)程
考慮到行業(yè)實(shí)際情況��,本指導(dǎo)原則不要求注冊(cè)申請(qǐng)人單獨(dú)建立醫(yī)療器械網(wǎng)絡(luò)安全生存周期(又稱生命周期)過(guò)程���,而是將其作為醫(yī)療器械軟件生存周期過(guò)程的重要組成部分予以整體考慮��,待時(shí)機(jī)成熟時(shí)予以考量。
注冊(cè)申請(qǐng)人需在醫(yī)療器械軟件生存周期過(guò)程考慮醫(yī)療器械網(wǎng)絡(luò)安全的質(zhì)控要求�����,并可基于醫(yī)療器械網(wǎng)絡(luò)安全能力建設(shè)要求予以實(shí)施����,具體要求詳見(jiàn)醫(yī)療器械軟件指導(dǎo)原則第六章以及獨(dú)立軟件生產(chǎn)質(zhì)量管理規(guī)范及其現(xiàn)場(chǎng)檢查指導(dǎo)原則。
同時(shí)�����,注冊(cè)申請(qǐng)人可參考信息安全領(lǐng)域相關(guān)標(biāo)準(zhǔn)和技術(shù)報(bào)告�,完善醫(yī)療器械網(wǎng)絡(luò)安全生存周期過(guò)程的質(zhì)控要求,本指導(dǎo)原則不再贅述���。
五�����、技術(shù)考量
(一)現(xiàn)成軟件
現(xiàn)成軟件同樣存在網(wǎng)絡(luò)安全問(wèn)題���,注冊(cè)申請(qǐng)人應(yīng)根據(jù)質(zhì)量管理體系要求建立現(xiàn)成軟件網(wǎng)絡(luò)安全更新過(guò)程,結(jié)合風(fēng)險(xiǎn)管理要求�����,及時(shí)將必要的現(xiàn)成軟件網(wǎng)絡(luò)安全信息及應(yīng)對(duì)措施告知用戶���。
同時(shí),根據(jù)現(xiàn)成軟件與醫(yī)療器械軟件的關(guān)系類型開(kāi)展相應(yīng)網(wǎng)絡(luò)安全質(zhì)控工作���。對(duì)于現(xiàn)成軟件組件(即作為醫(yī)療器械軟件組成部分的現(xiàn)成軟件)�,重點(diǎn)關(guān)注其網(wǎng)絡(luò)安全問(wèn)題對(duì)醫(yī)療器械使用效果的影響��,網(wǎng)絡(luò)安全的安全性級(jí)別判定亦需將其納入考量�����。對(duì)于外部軟件環(huán)境(即作為醫(yī)療器械軟件運(yùn)行環(huán)境組成部分的現(xiàn)成軟件),重點(diǎn)關(guān)注其網(wǎng)絡(luò)安全補(bǔ)丁對(duì)醫(yī)療器械安全有效性的影響��,網(wǎng)絡(luò)安全的安全性級(jí)別判定通常無(wú)需將其納入考量�����;需要說(shuō)明的是��,網(wǎng)絡(luò)安全補(bǔ)丁對(duì)于醫(yī)療器械而言屬于設(shè)計(jì)變更����,需對(duì)醫(yī)療器械進(jìn)行驗(yàn)證、確認(rèn)����。
(二)醫(yī)療數(shù)據(jù)出境
根據(jù)《中華人民共和國(guó)網(wǎng)絡(luò)安全法》《中華人民共和國(guó)數(shù)據(jù)安全法》《中華人民共和國(guó)個(gè)人信息保護(hù)法》《中華人民共和國(guó)人類遺傳資源管理?xiàng)l例》等法律法規(guī)相關(guān)規(guī)定,在中國(guó)境內(nèi)收集和產(chǎn)生的重要數(shù)據(jù)�����、個(gè)人信息和人類遺傳資源信息原則上應(yīng)在中國(guó)境內(nèi)存儲(chǔ)���,因業(yè)務(wù)需要確需向境外提供的,應(yīng)按照國(guó)家網(wǎng)信部門會(huì)同國(guó)務(wù)院有關(guān)部門制定的辦法進(jìn)行安全評(píng)估���。
《國(guó)家健康醫(yī)療大數(shù)據(jù)標(biāo)準(zhǔn)��、安全和服務(wù)管理辦法(試行)》明確:健康醫(yī)療大數(shù)據(jù)應(yīng)存儲(chǔ)在境內(nèi)安全可信的服務(wù)器上����,因業(yè)務(wù)需要確需向境外提供的,應(yīng)按照相關(guān)法律法規(guī)及有關(guān)要求進(jìn)行安全評(píng)估審核����。
醫(yī)療數(shù)據(jù)通常屬于重要數(shù)據(jù)[7],特別是敏感醫(yī)療數(shù)據(jù)含有個(gè)人信息���,因此醫(yī)療數(shù)據(jù)出境應(yīng)符合重要數(shù)據(jù)���、個(gè)人信息、人類遺傳資源信息出境安全評(píng)估相關(guān)規(guī)定�����。
(三)遠(yuǎn)程維護(hù)與升級(jí)
遠(yuǎn)程維護(hù)與升級(jí)雖為非醫(yī)療器械功能����,但會(huì)影響醫(yī)療器械的安全有效性,故亦需納入考量����。
具有遠(yuǎn)程維護(hù)與升級(jí)功能的醫(yī)療器械可訪問(wèn)和使用設(shè)備數(shù)據(jù)�,本身雖不涉及醫(yī)療數(shù)據(jù)��,但若未能實(shí)現(xiàn)設(shè)備數(shù)據(jù)和醫(yī)療數(shù)據(jù)的有效隔離��,則存在醫(yī)療數(shù)據(jù)未授權(quán)訪問(wèn)和使用以及被篡改的可能性�����。遠(yuǎn)程維護(hù)與升級(jí)所用電子接口也面臨網(wǎng)絡(luò)攻擊的威脅�����,可能會(huì)影響醫(yī)療器械正常運(yùn)行���,導(dǎo)致患者受到傷害或死亡以及隱私被侵犯���。醫(yī)療器械在遠(yuǎn)程維護(hù)與升級(jí)過(guò)程中若無(wú)人值守,則可能存在醫(yī)療器械非授權(quán)訪問(wèn)和使用的風(fēng)險(xiǎn)�。家用醫(yī)療器械的遠(yuǎn)程維護(hù)與升級(jí)需考慮其對(duì)產(chǎn)品正常使用的影響及其風(fēng)險(xiǎn)。
因此�����,注冊(cè)申請(qǐng)人需明確遠(yuǎn)程維護(hù)與升級(jí)的實(shí)現(xiàn)方法����、所用電子接口情況、設(shè)備數(shù)據(jù)所含內(nèi)容����、設(shè)備數(shù)據(jù)與醫(yī)療數(shù)據(jù)的隔離方法、網(wǎng)絡(luò)安全保證措施等技術(shù)特征�����,并提供相應(yīng)研究資料和風(fēng)險(xiǎn)管理資料�����。
此外��,境外遠(yuǎn)程維護(hù)與升級(jí)若可訪問(wèn)醫(yī)療數(shù)據(jù)�,亦應(yīng)符合醫(yī)療數(shù)據(jù)出境要求。
(四)遺留設(shè)備[8]
本指導(dǎo)原則所述遺留設(shè)備是指不能通過(guò)補(bǔ)丁更新����、補(bǔ)償控制等合理風(fēng)險(xiǎn)控制措施抵御當(dāng)前網(wǎng)絡(luò)安全威脅的醫(yī)療器械。遺留設(shè)備可能無(wú)法應(yīng)對(duì)當(dāng)前網(wǎng)絡(luò)安全威脅����,導(dǎo)致產(chǎn)品綜合剩余風(fēng)險(xiǎn)無(wú)法降至可接受水平��,降低醫(yī)療器械的安全有效性�����。
醫(yī)療器械實(shí)際使用情況極為復(fù)雜��,使得遺留設(shè)備的判定較為困難����。通常情況下可結(jié)合醫(yī)療器械的停售(EOL)��、停止售后服務(wù)(EOS)兩個(gè)時(shí)間點(diǎn)判定其是否屬于遺留設(shè)備:在售(以注冊(cè)證時(shí)效為準(zhǔn))的醫(yī)療器械均非遺留設(shè)備����;停售但未停止售后服務(wù)的醫(yī)療器械,若無(wú)法通過(guò)合理風(fēng)險(xiǎn)控制措施抵御當(dāng)前網(wǎng)絡(luò)安全威脅則為遺留設(shè)備�����,反之不屬于遺留設(shè)備�;停止售后服務(wù)的醫(yī)療器械均為遺留設(shè)備。
對(duì)于遺留設(shè)備�,注冊(cè)人應(yīng)按照質(zhì)量管理體系要求開(kāi)展相應(yīng)質(zhì)控工作����,以保證產(chǎn)品網(wǎng)絡(luò)安全�,詳見(jiàn)獨(dú)立軟件生產(chǎn)質(zhì)量管理規(guī)范及其現(xiàn)場(chǎng)檢查指導(dǎo)原則��。
對(duì)于注冊(cè)證失效但尚未停止售后服務(wù)�、注冊(cè)證有效但已停售的醫(yī)療器械,注冊(cè)人應(yīng)根據(jù)質(zhì)量管理體系要求向現(xiàn)有用戶提供必要的網(wǎng)絡(luò)安全相關(guān)信息以及應(yīng)對(duì)措施��,以保證醫(yī)療器械的網(wǎng)絡(luò)安全���。若無(wú)法保證醫(yī)療器械的網(wǎng)絡(luò)安全�����,按遺留設(shè)備處理���。
對(duì)于注冊(cè)證有效且在售的醫(yī)療器械,若無(wú)法通過(guò)合理風(fēng)險(xiǎn)控制措施抵御當(dāng)前網(wǎng)絡(luò)安全威脅����,則注冊(cè)人應(yīng)根據(jù)質(zhì)量管理體系要求制定相應(yīng)風(fēng)險(xiǎn)控制措施,并申請(qǐng)變更注冊(cè)�。
六����、醫(yī)療器械網(wǎng)絡(luò)安全研究資料
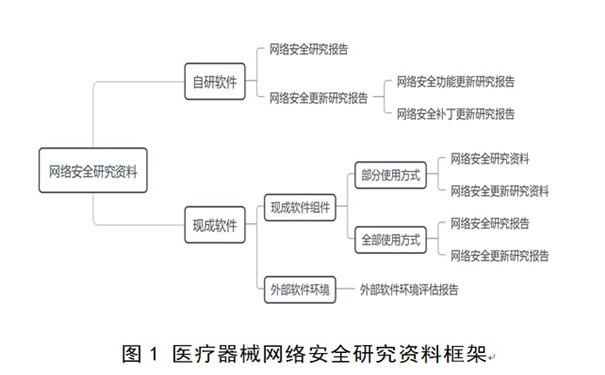
(一)自研軟件網(wǎng)絡(luò)安全研究報(bào)告
自研軟件網(wǎng)絡(luò)安全研究報(bào)告適用于自研軟件的初次發(fā)布和再次發(fā)布�����,內(nèi)容框架詳見(jiàn)表1�,包括基本信息、實(shí)現(xiàn)過(guò)程���、漏洞評(píng)估����、結(jié)論��,詳盡程度取決于軟件安全性級(jí)別��,不適用內(nèi)容詳述理由��。
1.基本信息
(1)軟件信息
明確申報(bào)醫(yī)療器械軟件的名稱����、型號(hào)規(guī)格、發(fā)布版本以及軟件安全性級(jí)別。
若網(wǎng)絡(luò)安全的安全性級(jí)別低于軟件的安全性級(jí)別���,詳述理由并按網(wǎng)絡(luò)安全的安全性級(jí)別提交相應(yīng)注冊(cè)申報(bào)資料��。
(2)數(shù)據(jù)架構(gòu)
提供申報(bào)醫(yī)療器械在每個(gè)使用場(chǎng)景(含遠(yuǎn)程維護(hù)與升級(jí)�,下同)下的網(wǎng)絡(luò)環(huán)境和數(shù)據(jù)流圖�,并依據(jù)圖示描述醫(yī)療器械相關(guān)數(shù)據(jù)和電子接口的基本情況。
數(shù)據(jù)情況明確醫(yī)療器械相關(guān)數(shù)據(jù)的類型(敏感醫(yī)療數(shù)據(jù)�����、非敏感醫(yī)療數(shù)據(jù)����、設(shè)備數(shù)據(jù))����,并依據(jù)數(shù)據(jù)類型明確每類數(shù)據(jù)的具體內(nèi)容(如個(gè)人信息、醫(yī)療活動(dòng)信息��、設(shè)備運(yùn)行信息)����、功能(如單向、雙向電子數(shù)據(jù)交換,實(shí)時(shí)�����、非實(shí)時(shí)遠(yuǎn)程訪問(wèn)與控制)��、用途(如醫(yī)療活動(dòng)�����、設(shè)備維護(hù))等���。
電子接口情況逐項(xiàng)說(shuō)明每個(gè)網(wǎng)絡(luò)接口�、電子數(shù)據(jù)交換接口的預(yù)期用戶�、使用場(chǎng)景、預(yù)期用途��、數(shù)據(jù)類型����、技術(shù)特征、使用限制���,其中技術(shù)特征要求詳見(jiàn)第二章����。
(3)網(wǎng)絡(luò)安全能力
基于第二章所述各項(xiàng)網(wǎng)絡(luò)安全能力,逐項(xiàng)分析申報(bào)醫(yī)療器械對(duì)于該項(xiàng)網(wǎng)絡(luò)安全能力的適用性���,詳述適用網(wǎng)絡(luò)安全能力的實(shí)現(xiàn)方法以及不適用理由���。若適用,提供其他網(wǎng)絡(luò)安全能力的適用情況說(shuō)明���。
(4)網(wǎng)絡(luò)安全補(bǔ)丁
提供申報(bào)醫(yī)療器械(含必備軟件���、外部軟件環(huán)境)的網(wǎng)絡(luò)安全補(bǔ)丁列表�,明確網(wǎng)絡(luò)安全補(bǔ)丁的名稱、完整版本����、發(fā)布日期??闪砀轿募?/p>
(5)安全軟件
描述申報(bào)醫(yī)療器械兼容或所用的安全軟件(如殺毒軟件���、防火墻等)的名稱���、型號(hào)規(guī)格��、完整版本��、供應(yīng)商��、運(yùn)行環(huán)境����、防護(hù)規(guī)則配置要求����。
2.實(shí)現(xiàn)過(guò)程
(1)風(fēng)險(xiǎn)管理
提供申報(bào)醫(yī)療器械網(wǎng)絡(luò)安全的風(fēng)險(xiǎn)分析報(bào)告、風(fēng)險(xiǎn)管理報(bào)告����,另附網(wǎng)絡(luò)安全開(kāi)發(fā)所形成的原始文件。亦可提供醫(yī)療器械軟件的風(fēng)險(xiǎn)管理文檔���,但需注明網(wǎng)絡(luò)安全情況���。
(2)需求規(guī)范
提供申報(bào)醫(yī)療器械的網(wǎng)絡(luò)安全需求規(guī)范文檔,另附網(wǎng)絡(luò)安全開(kāi)發(fā)所形成的原始文件�����。亦可提供醫(yī)療器械軟件的需求規(guī)范文檔,但需注明網(wǎng)絡(luò)安全情況���。
(3)驗(yàn)證與確認(rèn)
提供申報(bào)醫(yī)療器械的網(wǎng)絡(luò)安全測(cè)試計(jì)劃和報(bào)告�����,另附網(wǎng)絡(luò)安全開(kāi)發(fā)所形成的原始文件�����。亦可提供醫(yī)療器械軟件的系統(tǒng)測(cè)試計(jì)劃和報(bào)告�����,但需注明網(wǎng)絡(luò)安全情況�����。
對(duì)于安全軟件,提供兼容性測(cè)試報(bào)告�。對(duì)于標(biāo)準(zhǔn)傳輸協(xié)議或存儲(chǔ)格式,若其滿足醫(yī)療器械網(wǎng)絡(luò)安全需求出具真實(shí)性聲明即可���,反之提供相應(yīng)證明材料�����;對(duì)于私有傳輸協(xié)議或存儲(chǔ)格式��,提供完整性測(cè)試總結(jié)報(bào)告����。對(duì)于實(shí)時(shí)遠(yuǎn)程訪問(wèn)與控制功能,提供完整性和可得性等網(wǎng)絡(luò)安全特性的測(cè)試報(bào)告�����。對(duì)于醫(yī)用無(wú)線專用設(shè)備�����,提供符合無(wú)線電管理相關(guān)規(guī)定的證明材料���。
(4)可追溯性分析
提供申報(bào)醫(yī)療器械的網(wǎng)絡(luò)安全可追溯性分析報(bào)告��,匯總列明網(wǎng)絡(luò)安全需求規(guī)范文檔���、網(wǎng)絡(luò)安全設(shè)計(jì)規(guī)范文檔��、源代碼(明確軟件單元名稱即可)�����、網(wǎng)絡(luò)安全測(cè)試報(bào)告�、網(wǎng)絡(luò)安全風(fēng)險(xiǎn)分析報(bào)告之間的對(duì)應(yīng)關(guān)系�。亦可提供醫(yī)療器械軟件的可追溯性報(bào)告,但需注明網(wǎng)絡(luò)安全情況����。
(5)維護(hù)計(jì)劃
輕微級(jí)別:提供申報(bào)醫(yī)療器械網(wǎng)絡(luò)安全更新的流程圖,并依據(jù)圖示描述相關(guān)活動(dòng)��。
中等���、嚴(yán)重級(jí)別:在輕微級(jí)別的基礎(chǔ)上���,提供網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)的流程圖,并依據(jù)圖示描述相關(guān)活動(dòng)��;或者提供網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)預(yù)案文檔���。
若適用�,全部級(jí)別均需提供遠(yuǎn)程維護(hù)與升級(jí)的流程圖�,并依據(jù)圖示描述相關(guān)活動(dòng)。
3.漏洞評(píng)估
輕微級(jí)別:按照現(xiàn)行有效的通用漏洞評(píng)分系統(tǒng)(CVSS)所定義的漏洞等級(jí)����,明確申報(bào)醫(yī)療器械(含必備軟件、外部軟件環(huán)境���,下同)已知漏洞總數(shù)和已知剩余漏洞數(shù)��。
中等級(jí)別:提供網(wǎng)絡(luò)安全漏洞自評(píng)報(bào)告���,明確漏洞掃描所用軟件工具、漏洞庫(kù)(基于國(guó)家信息安全漏洞庫(kù)或互認(rèn)的國(guó)際信息安全漏洞庫(kù))的基本信息(如名稱�、完整版本、發(fā)布日期��、供應(yīng)商等)�����,按照CVSS漏洞等級(jí)明確申報(bào)醫(yī)療器械已知漏洞總數(shù)和已知剩余漏洞數(shù)�����,列明已知剩余漏洞的內(nèi)容、對(duì)產(chǎn)品的影響及綜合剩余風(fēng)險(xiǎn)���,確保產(chǎn)品綜合剩余風(fēng)險(xiǎn)均可接受�����。亦可補(bǔ)充網(wǎng)絡(luò)安全評(píng)估機(jī)構(gòu)出具的網(wǎng)絡(luò)安全漏洞評(píng)估報(bào)告�����。
嚴(yán)重級(jí)別:提供網(wǎng)絡(luò)安全漏洞自評(píng)報(bào)告��、網(wǎng)絡(luò)安全評(píng)估機(jī)構(gòu)出具的網(wǎng)絡(luò)安全漏洞評(píng)估報(bào)告�����,明確已知剩余漏洞的維護(hù)方案����,確保產(chǎn)品綜合剩余風(fēng)險(xiǎn)均可接受�����。
4.結(jié)論
概述申報(bào)醫(yī)療器械的網(wǎng)絡(luò)安全實(shí)現(xiàn)過(guò)程的規(guī)范性和網(wǎng)絡(luò)安全漏洞評(píng)估結(jié)果,判定申報(bào)醫(yī)療器械的網(wǎng)絡(luò)安全是否滿足要求���,受益是否大于風(fēng)險(xiǎn)。
表1 自研軟件網(wǎng)絡(luò)安全研究報(bào)告框架
報(bào)告條款 | 軟件安全性級(jí)別 |
輕微 | 中等 | 嚴(yán)重 |
基本信息 | 軟件信息 | 明確軟件的基本情況和安全性級(jí)別 |
數(shù)據(jù)架構(gòu) | 提供每個(gè)使用場(chǎng)景的網(wǎng)絡(luò)環(huán)境和數(shù)據(jù)流圖����,描述醫(yī)療器械相關(guān)數(shù)據(jù)和電子接口的基本情況 |
網(wǎng)絡(luò)安全能力 | 明確網(wǎng)絡(luò)安全能力情況 |
網(wǎng)絡(luò)安全補(bǔ)丁 | 列明網(wǎng)絡(luò)安全補(bǔ)丁的基本情況 |
安全軟件 | 明確安全軟件的基本情況 |
實(shí)現(xiàn)過(guò)程 | 風(fēng)險(xiǎn)管理 | 提供網(wǎng)絡(luò)安全的風(fēng)險(xiǎn)分析報(bào)告、風(fēng)險(xiǎn)管理報(bào)告 |
需求規(guī)范 | 提供網(wǎng)絡(luò)安全需求規(guī)范文檔 |
驗(yàn)證與確認(rèn) | 提供網(wǎng)絡(luò)安全的測(cè)試計(jì)劃和報(bào)告 |
可追溯性分析 | 提供網(wǎng)絡(luò)安全可追溯性分析報(bào)告 |
維護(hù)計(jì)劃 | 提供網(wǎng)絡(luò)安全更新��、遠(yuǎn)程維護(hù)與升級(jí)的流程圖及活動(dòng)描述 | 提供網(wǎng)絡(luò)安全更新�、網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)、遠(yuǎn)程維護(hù)與升級(jí)的流程圖及活動(dòng)描述 |
漏洞評(píng)估 | 按照漏洞等級(jí)明確已知漏洞總數(shù)和剩余漏洞數(shù) | 提供網(wǎng)絡(luò)安全漏洞自評(píng)報(bào)告�����,按照漏洞等級(jí)明確已知漏洞總數(shù)�、已知剩余漏洞情況 | 提供網(wǎng)絡(luò)安全漏洞自評(píng)報(bào)告、網(wǎng)絡(luò)安全評(píng)估機(jī)構(gòu)出具的網(wǎng)絡(luò)安全漏洞評(píng)估報(bào)告���,明確已知剩余漏洞的維護(hù)方案 |
結(jié)論 | 概述網(wǎng)絡(luò)安全實(shí)現(xiàn)過(guò)程的規(guī)范性和網(wǎng)絡(luò)安全漏洞評(píng)估結(jié)果��,判定網(wǎng)絡(luò)安全是否滿足要求 |
(二)自研軟件網(wǎng)絡(luò)安全更新研究報(bào)告
自研軟件網(wǎng)絡(luò)安全更新研究報(bào)告適用于自研軟件的再次發(fā)布�����,包括網(wǎng)絡(luò)安全功能更新����、網(wǎng)絡(luò)安全補(bǔ)丁更新等研究報(bào)告。
網(wǎng)絡(luò)安全功能更新研究報(bào)告適用于自研軟件發(fā)生重大����、輕微網(wǎng)絡(luò)安全功能更新,或合并網(wǎng)絡(luò)安全補(bǔ)丁更新的情形���,內(nèi)容框架詳見(jiàn)表2��,不再贅述���。
網(wǎng)絡(luò)安全補(bǔ)丁更新研究報(bào)告適用于自研軟件(含必備軟件、外部軟件環(huán)境)僅發(fā)生網(wǎng)絡(luò)安全補(bǔ)丁更新的情形�����。其內(nèi)容包括軟件信息���、網(wǎng)絡(luò)安全補(bǔ)丁��、風(fēng)險(xiǎn)管理�����、驗(yàn)證與確認(rèn)����、可追溯性分析����、維護(hù)計(jì)劃、漏洞評(píng)估�、結(jié)論,具體要求詳見(jiàn)表2相應(yīng)說(shuō)明���。
表2 自研軟件網(wǎng)絡(luò)安全功能更新研究報(bào)告框架
報(bào)告條款 | 軟件安全性級(jí)別 |
輕微 | 中等 | 嚴(yán)重 |
基本信息 | 軟件信息 | 明確本次申報(bào)軟件情況�,詳述變化 |
數(shù)據(jù)架構(gòu) | 明確本次申報(bào)軟件情況���,詳述變化 |
網(wǎng)絡(luò)安全能力 | 明確本次申報(bào)軟件情況���,詳述變化 |
網(wǎng)絡(luò)安全補(bǔ)丁 | 列明網(wǎng)絡(luò)安全更新部分的補(bǔ)丁情況 |
安全軟件 | 明確本次申報(bào)軟件情況,詳述變化 |
實(shí)現(xiàn)過(guò)程 | 風(fēng)險(xiǎn)管理 | 提供網(wǎng)絡(luò)安全更新部分的風(fēng)險(xiǎn)分析報(bào)告��、風(fēng)險(xiǎn)管理報(bào)告 |
需求規(guī)范 | 提供網(wǎng)絡(luò)安全更新部分需求規(guī)范文檔 |
驗(yàn)證與確認(rèn) | 提供網(wǎng)絡(luò)安全更新部分的測(cè)試計(jì)劃和報(bào)告 |
可追溯性分析 | 提供網(wǎng)絡(luò)安全更新部分的可追溯性分析報(bào)告 |
維護(hù)計(jì)劃 | 提供用戶告知計(jì)劃 | 提供用戶告知計(jì)劃����、網(wǎng)絡(luò)安全事件應(yīng)急響應(yīng)總結(jié)報(bào)告 |
漏洞評(píng)估 | 明確本次申報(bào)軟件已知漏洞總數(shù)和剩余漏洞數(shù) | 提供本次申報(bào)軟件的網(wǎng)絡(luò)安全自評(píng)報(bào)告�����,按照漏洞等級(jí)明確已知漏洞總數(shù)��、已知剩余漏洞情況 | 提供本次申報(bào)軟件的網(wǎng)絡(luò)安全自評(píng)報(bào)告���、網(wǎng)絡(luò)安全評(píng)估機(jī)構(gòu)出具的網(wǎng)絡(luò)安全漏洞評(píng)估報(bào)告,明確已知剩余漏洞的維護(hù)方案 |
結(jié)論 | 概述網(wǎng)絡(luò)安全更新實(shí)現(xiàn)過(guò)程的規(guī)范性和網(wǎng)絡(luò)安全漏洞評(píng)估結(jié)果�,判定網(wǎng)絡(luò)安全更新是否滿足要求 |
考慮到網(wǎng)絡(luò)安全更新具有累積效應(yīng),網(wǎng)絡(luò)安全更新研究報(bào)告需涵蓋醫(yī)療器械軟件自前次注冊(cè)(延續(xù)注冊(cè)除外)以來(lái)網(wǎng)絡(luò)安全更新的全部?jī)?nèi)容���。
(三)現(xiàn)成軟件網(wǎng)絡(luò)安全研究資料
1.現(xiàn)成軟件組件網(wǎng)絡(luò)安全研究資料
(1)部分使用方式
對(duì)于部分使用方式����,即醫(yī)療器械軟件同時(shí)使用自研軟件和現(xiàn)成軟件組件�,無(wú)需單獨(dú)提交網(wǎng)絡(luò)安全研究報(bào)告,基于醫(yī)療器械軟件的安全性級(jí)別���,在自研軟件網(wǎng)絡(luò)安全研究報(bào)告適用條款中說(shuō)明現(xiàn)成軟件組件的情況�。
適用條款包括軟件信息����、數(shù)據(jù)架構(gòu)�����、網(wǎng)絡(luò)安全能力��、網(wǎng)絡(luò)安全補(bǔ)丁����、風(fēng)險(xiǎn)管理�����、需求規(guī)范�、驗(yàn)證與確認(rèn)�、可追溯性分析、維護(hù)計(jì)劃�、漏洞評(píng)估、結(jié)論�。
此時(shí)若現(xiàn)成軟件組件發(fā)生網(wǎng)絡(luò)安全更新,網(wǎng)絡(luò)安全功能更新在自研軟件網(wǎng)絡(luò)安全功能更新研究報(bào)告的基礎(chǔ)上��,說(shuō)明現(xiàn)成軟件組件的變化情況�,不適用條款說(shuō)明理由���;網(wǎng)絡(luò)安全補(bǔ)丁更新要求與自研軟件相同。
(2)全部使用方式
對(duì)于全部使用方式�,即醫(yī)療器械軟件全部為現(xiàn)成軟件組件,需要單獨(dú)提交現(xiàn)成軟件組件網(wǎng)絡(luò)安全研究報(bào)告���,其內(nèi)容與自研軟件研究報(bào)告相同����,但需基于現(xiàn)成軟件組件(此時(shí)即醫(yī)療器械軟件)的安全性級(jí)別予以說(shuō)明����。
此時(shí)若現(xiàn)成軟件組件發(fā)生網(wǎng)絡(luò)安全更新,網(wǎng)絡(luò)安全功能更新在現(xiàn)成軟件組件網(wǎng)絡(luò)安全功能更新研究報(bào)告的基礎(chǔ)上��,說(shuō)明現(xiàn)成軟件組件的變化情況����,不適用條款說(shuō)明理由;網(wǎng)絡(luò)安全補(bǔ)丁更新要求與自研軟件相同�����。
2.外部軟件環(huán)境網(wǎng)絡(luò)安全評(píng)估資料
外部軟件環(huán)境網(wǎng)絡(luò)安全評(píng)估作為外部軟件環(huán)境評(píng)估的重要組成部分����,其網(wǎng)絡(luò)安全及其更新的研究資料要求與外部軟件環(huán)境評(píng)估報(bào)告相同�,具體要求詳見(jiàn)醫(yī)療器械軟件指導(dǎo)原則第八章�����。
考慮到醫(yī)療器械軟件指導(dǎo)原則已明確外部軟件環(huán)境評(píng)估報(bào)告要求�,同時(shí)自研軟件網(wǎng)絡(luò)安全研究資料亦含有外部軟件環(huán)境的網(wǎng)絡(luò)安全補(bǔ)丁、漏洞評(píng)估等要求����,故無(wú)需單獨(dú)提交外部軟件環(huán)境網(wǎng)絡(luò)安全評(píng)估資料。
七�����、注冊(cè)申報(bào)資料補(bǔ)充說(shuō)明[9]
注冊(cè)申報(bào)資料在符合醫(yī)療器械注冊(cè)申報(bào)資料要求等文件要求基礎(chǔ)上��,滿足醫(yī)療器械軟件等相關(guān)指導(dǎo)原則要求��,同時(shí)重點(diǎn)關(guān)注以下要求�。
(一)產(chǎn)品注冊(cè)
1.軟件研究資料
在軟件研究資料中單獨(dú)提交自研軟件網(wǎng)絡(luò)安全研究報(bào)告���。
若使用現(xiàn)成軟件組件���,根據(jù)其使用方式提交相應(yīng)研究資料����。相關(guān)研究資料的具體要求詳見(jiàn)第六章��。
2.說(shuō)明書(shū)
說(shuō)明書(shū)提供網(wǎng)絡(luò)安全說(shuō)明和使用指導(dǎo)�����,明確用戶訪問(wèn)控制機(jī)制��、電子接口(含網(wǎng)絡(luò)接口����、電子數(shù)據(jù)交換接口)及其數(shù)據(jù)類型和技術(shù)特征、網(wǎng)絡(luò)安全特征配置���、數(shù)據(jù)備份與災(zāi)難恢復(fù)�、運(yùn)行環(huán)境(含硬件配置����、外部軟件環(huán)境、網(wǎng)絡(luò)環(huán)境,若適用)�、安全軟件兼容性列表(若適用)、外部軟件環(huán)境與安全軟件更新(若適用)��、現(xiàn)成軟件清單(SBOM�,若適用)等要求。
(二)變更注冊(cè)
1.軟件研究資料
醫(yī)療器械變更注冊(cè)應(yīng)根據(jù)網(wǎng)絡(luò)安全更新情況��,提交變化部分對(duì)產(chǎn)品安全性與有效性影響的研究資料:
(1)涉及網(wǎng)絡(luò)安全功能更新:適用于自研軟件發(fā)生網(wǎng)絡(luò)安全功能更新���,或合并網(wǎng)絡(luò)安全補(bǔ)丁更新的情形���,此時(shí)單獨(dú)提交一份自研軟件網(wǎng)絡(luò)安全功能更新研究報(bào)告(或自研軟件網(wǎng)絡(luò)安全研究報(bào)告);
(2)僅發(fā)生網(wǎng)絡(luò)安全補(bǔ)丁更新:適用于自研軟件(含必備軟件�、外部軟件環(huán)境)僅發(fā)生網(wǎng)絡(luò)安全補(bǔ)丁更新的情形,此時(shí)單獨(dú)提交一份自研軟件網(wǎng)絡(luò)安全補(bǔ)丁更新研究報(bào)告����;
(3)未發(fā)生網(wǎng)絡(luò)安全更新:出具真實(shí)性聲明,明確對(duì)此承擔(dān)法律責(zé)任��。
若使用現(xiàn)成軟件組件�,根據(jù)其使用方式提交相應(yīng)研究資料����。相關(guān)研究資料的具體要求詳見(jiàn)第六章�����。
2.說(shuō)明書(shū)
若適用�����,提交說(shuō)明書(shū)關(guān)于網(wǎng)絡(luò)安全內(nèi)容的變更對(duì)比表��。
(三)延續(xù)注冊(cè)
延續(xù)注冊(cè)通常無(wú)需提交網(wǎng)絡(luò)安全相關(guān)研究資料�����。若適用�����,根據(jù)注冊(cè)證“備注”所載明的要求提交相應(yīng)網(wǎng)絡(luò)安全研究資料�����。
產(chǎn)品技術(shù)要求“產(chǎn)品型號(hào)/規(guī)格及其劃分說(shuō)明”所述軟件版本命名規(guī)則應(yīng)涵蓋網(wǎng)絡(luò)安全更新情況�,區(qū)分重大網(wǎng)絡(luò)安全更新和輕微網(wǎng)絡(luò)安全更新�����。若原注冊(cè)產(chǎn)品標(biāo)準(zhǔn)(或原產(chǎn)品技術(shù)要求)及其變更對(duì)比表未體現(xiàn)軟件相關(guān)信息,需在符合性聲明中予以明確����,其中軟件版本命名規(guī)則需涵蓋網(wǎng)絡(luò)安全更新情況。
八�����、參考文獻(xiàn)
[1] 全國(guó)人大. 中華人民共和國(guó)網(wǎng)絡(luò)安全法[Z]��,2016.11
[2] 全國(guó)人大. 中華人民共和國(guó)數(shù)據(jù)安全法[Z]�,2021.6
[3] 全國(guó)人大. 中華人民共和國(guó)個(gè)人信息保護(hù)法[Z],2021.8
[4] 國(guó)務(wù)院. 中華人民共和國(guó)人類遺傳資源管理?xiàng)l例(國(guó)令第717號(hào))[Z]����,2019.5
[5] 中央網(wǎng)信辦. 國(guó)家網(wǎng)絡(luò)安全事件應(yīng)急預(yù)案[Z],2017.1
[6] 國(guó)家網(wǎng)信辦. 個(gè)人信息出境安全評(píng)估辦法(征求意見(jiàn)稿)[Z]����,2019.6
[7] 國(guó)家網(wǎng)信辦. 數(shù)據(jù)出境安全評(píng)估辦法(征求意見(jiàn)稿)[Z],2021.10
[8] 國(guó)家網(wǎng)信辦. 網(wǎng)絡(luò)安全審查辦法[Z]���,2021.11
[9] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定(總局令第6號(hào))[Z],2014.7
[10] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械召回管理辦法(總局令第29號(hào))[Z],2017.1
[11] 國(guó)家市場(chǎng)監(jiān)督管理總局. 醫(yī)療器械不良事件監(jiān)測(cè)和再評(píng)價(jià)管理辦法(總局令第1號(hào))[Z]�,2018.8
[12] 國(guó)家市場(chǎng)監(jiān)督管理總局.醫(yī)療器械注冊(cè)與備案管理辦法(總局令第47號(hào))[Z],2021.8
[13] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范(2014年第64號(hào)公告)[Z]���,2014.12
[14] 國(guó)家市場(chǎng)監(jiān)督管理總局.醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式(2021年第121號(hào)公告)[Z]����,2021.9
[15] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)技術(shù)審查指導(dǎo)原則(2017年第13號(hào)通告)[Z]���,2017.1
[16] 國(guó)家藥品監(jiān)督管理局.醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范附錄獨(dú)立軟件(2019年第43號(hào)通告)[Z]�,2019.7
[17] 國(guó)家藥品監(jiān)督管理局.醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范獨(dú)立軟件現(xiàn)場(chǎng)檢查指導(dǎo)原則(藥監(jiān)綜械管〔2020〕57號(hào))[Z]�����,2020.5
[18] 國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心. 醫(yī)療器械軟件技術(shù)審查指導(dǎo)原則(第二版)(征求意見(jiàn)稿)[Z]�,2020.5
[19] 北京市藥品監(jiān)督管理局. 醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)審查指導(dǎo)原則實(shí)施指南[Z],2019.12
[20]國(guó)家衛(wèi)生健康委員會(huì). 國(guó)家健康醫(yī)療大數(shù)據(jù)標(biāo)準(zhǔn)�����、安全和服務(wù)管理辦法(試行)(國(guó)衛(wèi)規(guī)劃發(fā)〔2018〕23號(hào))[Z]�����,2018.7
[21] GB9706.1-2020 醫(yī)用電氣設(shè)備 第1部分:基本安全和基本性能的通用要求[S]
[22] GB/T 20985.1-2017 信息技術(shù) 安全技術(shù) 信息安全事件管理 第1部分:事件管理原理[S]
[23] GB/T 22080-2016信息技術(shù)安全技術(shù)信息安全管理體系要求[S]
[24] GB/T 22081-2016信息技術(shù)安全技術(shù)信息安全管理實(shí)用規(guī)則[S]
[25] GB/T 22239-2019 信息安全技術(shù) 網(wǎng)絡(luò)安全等級(jí)保護(hù)基本要求[S]
[26] GB/T 25000.51-2016系統(tǒng)與軟件工程 系統(tǒng)與軟件質(zhì)量要求和評(píng)價(jià)(SQuaRE) 第51部分:就緒可用軟件產(chǎn)品(RUSP)的質(zhì)量要求和測(cè)試細(xì)則[S]
[27] GB/T 25070-2019 信息安全技術(shù) 網(wǎng)絡(luò)安全等級(jí)保護(hù)安全設(shè)計(jì)技術(shù)要求[S]
[28] GB/T 28448-2019 信息安全技術(shù) 網(wǎng)絡(luò)安全等級(jí)保護(hù)測(cè)評(píng)要求[S]
[29] GB/T 29246-2017 信息技術(shù)安全技術(shù)信息安全管理體系概述和詞匯[S]
[30] GB/T 30276-2020信息安全技術(shù) 網(wǎng)絡(luò)安全漏洞管理規(guī)范[S]
[31] GB/T 31167-2014信息安全技術(shù) 云計(jì)算服務(wù)安全指南[S]
[32] GB/T 31168-2014信息安全技術(shù) 云計(jì)算服務(wù)安全能力要求[S]
[33] GB/T 31722-2015 信息技術(shù) 安全技術(shù) 信息安全風(fēng)險(xiǎn)管理[S]
[34] GB/T 35273-2020信息安全技術(shù) 個(gè)人信息安全規(guī)范[S]
[35] GB/T 35274-2017信息安全技術(shù) 大數(shù)據(jù)服務(wù)安全能力要求[S]
[36] GB/T 35278-2017信息安全技術(shù) 移動(dòng)終端安全保護(hù)技術(shù)要求[S]
[37] GB/T 37964-2019信息安全技術(shù) 個(gè)人信息去標(biāo)識(shí)化指南[S]
[38] GB/T 37973-2019信息安全技術(shù) 大數(shù)據(jù)安全管理指南[S]
[39] GB/T 37988-2019信息安全技術(shù) 數(shù)據(jù)安全能力成熟度模型[S]
[40] GB/T 39335-2020信息安全技術(shù) 個(gè)人信息安全影響評(píng)估指南[S]
[41] GB/T 39725-2020信息安全技術(shù) 健康醫(yī)療數(shù)據(jù)安全指南[S]
[42] GB/T信息安全技術(shù) 數(shù)據(jù)出境安全評(píng)估指南(征求意見(jiàn)稿)[S],2017.8
[43] GB/T信息安全技術(shù) 重要數(shù)據(jù)識(shí)別指南(征求意見(jiàn)稿)[S]�,2022.1
[44] YY/T 0287-2017 醫(yī)療器械 質(zhì)量管理體系 用于法規(guī)的要求[S]
[45] YY/T 0316-2016醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用[S]
[46] YY/T 0664-2020 醫(yī)療器械軟件 軟件生存周期過(guò)程[S]
[47] YY/T 1406.1-2016醫(yī)療器械軟件 第1部分:YY/T 0316應(yīng)用于醫(yī)療器械軟件的指南[S]
[48] YY/T 1708.1-2020醫(yī)用診斷X射線影像設(shè)備連通性符合性基本要求 第1部分:通用要求[S]
[49] YY/T 1708.2-2020醫(yī)用診斷X射線影像設(shè)備連通性符合性基本要求 第2部分:X射線計(jì)算機(jī)體層攝影設(shè)備[S]
[50] YY/T 1708.3-2021 醫(yī)用診斷X射線影像設(shè)備連通性符合性基本要求 第3部分:數(shù)字化攝影X射線機(jī)(DR)[S]
[51] YY/T 1708.4-2021 醫(yī)用X射線影像設(shè)備連通性符合性基本要求 第4 部分:數(shù)字減影血管造影X射線機(jī)(DSA)[S]
[52] YY/T 1708.5-2021 醫(yī)用診斷X射線影像設(shè)備連通性符合性基本要求 第5 部分:乳腺X射線機(jī)[S]
[53] YY/T 1708.6-2021 醫(yī)用診斷X射線影像設(shè)備連通性符合性基本要求 第6 部分:口腔X射線機(jī)[S]
[54] YY/T 醫(yī)用電氣設(shè)備網(wǎng)絡(luò)安全基本要求(報(bào)批稿)[S],2020.12
[55] IMDRF/SaMD WG/N12 FINAL: 2014, SaMD:Possible Framework for Risk Categorization and Corresponding Considerations[Z], 2014.9
[56] IMDRF/SaMD WG/N23 FINAL:2015,SaMD:Application of Quality Management System[Z], 2015.10
[57] IMDRF/CYBER WG/N60FINAL:2020, Principles and Practices for Medical Device Cybersecurity[Z], 2020.4
[58] FDA, Cybersecurity for Networked Medical Devices Containing Off-the-Shelf Software[Z], 2005.1
[59] FDA, Content of Premarket Submissions for Management of Cybersecurity in Medical Devices[Z], 2014.10
[60] FDA, Postmarket Management of Cybersecurity in Medical Devices[Z], 2016.12
[61] FDA, Design Considerations and Pre-market Submission Recommendations for Interoperable Medical Devices[Z], 2017.9
[62] FDA, Content of Premarket Submissions for Management of Cybersecurity in Medical Devices(Draft Guidance)[Z], 2018.10
[63] FDA, Best Practices for Communicating Cybersecurity Vulnerabilities to Patients[Z], 2021.10
[64] FDA, Playbook for Threat Modeling Medical Devices[Z], 2021.11
[65] MDCG 2019-16 Rev.1, Guidance on Cybersecurity for medical devices[Z], 2020.7
[66] BSI. Cybersecurity of medical devices:Addressing patient safety and the security of patient health information[Z], 2017.3
[67] AAMI TIR57:2016/(R)2019, Principles for medical device security - Risk management[S]
[68] AAMI TIR97:2019, Principles for medical device security - Postmarket risk management for device manufacturers[S]
[69] IEC TR 60601-4-5:2021, Medical electrical equipment - Part 4-5:Guidance and interpretation - Safety-related technical security specifications[S]
[70] IEC80001-1:2021, Application of risk management for IT-networks incorporating medical devices - Part 1:Safety, effectiveness and security in the implementation and use of connected medical devices or connected health software[S]
[71] IECTR 80001-2-1:2012, Application of risk management for IT-networks incorporating medical devices - Part 2-1: Step-by-step risk management of medical IT-networks - Practical applications and examples[S]
[72] IECTR 80001-2-2:2012, Application of risk management for IT-networks incorporating medical devices - Part 2-2: Guidance for the disclosure and communication of medical device security needs, risks and controls[S]
[73] IECTR 80001-2-3:2012, Application of risk management for IT-networks incorporating medical devices - Part 2-3: Guidance for wireless networks[S]
[74] IECTR 80001-2-4:2012, Application of risk management for IT-networks incorporating medical devices - Part 2-4: Application guidance - General implementation guidance for healthcare delivery organizations[S]
[75] IECTR 80001-2-5:2014, Application of risk management for IT-networks incorporating medical devices - Part 2-5: Application guidance - Guidance on distributed alarm systems[S]
[76] ISOTR 80001-2-6:2014, Application of risk management for IT-networks incorporating medical devices -Part 2-6: Application guidance - Guidance for responsibility agreements[S]
[77] ISOTR 80001-2-7:2015, Application of risk management for IT-networks incorporating medical devices -Application guidance -Part 2-7: Guidance for Healthcare Delivery Organizations (HDOs) on how to self-assess their conformance with IEC 80001-1[S]
[78] IECTR 80001-2-8:2016, Application of risk management for IT-networks incorporating medical devices - Part 2-8: Application guidance - Guidance on standards for establishing the security capabilities identified in IEC/TR 80001-2-2[S]
[79] IECTR 80001-2-9:2017, Application of risk management for IT-networks incorporating medical devices - Part 2-9: Application guidance - Guidance for use of security assurance cases to demonstrate confidence in IEC/TR 80001-2-2 security capabilities[S]
[80] IEC 80001-5-1:2021,Health software and health IT systems safety, effectiveness and security - Part 5-1: Security - Activities in the product life cycle[S]
[81] ISO 81001-1:2021, Health software and health IT systems safety, effectiveness and security - Part 1: Principles and concepts[S]
[82] ISO TS 81001-2-1, Health software and health IT systems safety,effectiveness and security - Part 2-1:Coordination - Guidance for the use of assurance cases for safety and security[S]
[83] ISO/IEC 27035-1:2016, Information technology - Security techniques - Information security incident management - Part 1: Principles of incident management[S]
[84] ISO/IEC 27035-2:2016, Information technology - Security techniques - Information security incident management - Part 2: Guidelines to plan and prepare for incident response[S]
[85] ISO/IEC 29147:2018, Information Technology - Security Techniques - Vulnerability Disclosure[S]
[86] ISO/IEC 30111:2013, Information Technology - Security Techniques - Vulnerability Handling Processes[S]
[87] ISO 27799:2016, Health informatics - Information security management in health using ISO/IEC 27002[S]
[88] NEMA CSP 1-2016, Cybersecurity for Medical Imaging[S]
[89] NEMA HN 1-2019, Manufacturer Disclosure Statement for Medical Device Security[S]
[90] UL 2900-1:2020, Standard for Software Cybersecurity for Network Connectable Products - Part 1: General Requirements[S]
[91] UL 2900-2-1:2018, Software Cybersecurity for Network Connectable Products - Part 2-1: Particular Requirements for Network Connectable Components of Healthcare and Wellness Systems[S]